若年性アルツハイマー病におけるレカネマブの効果 [アルツハイマー病]
64歳以下の方から「レカネマブによる治療を検討した方が良いですか?」と相談されたとき用のパンフレット(自作)
レカネマブ(レケンビ![[レジスタードトレードマーク]](https://blog.ss-blog.jp/_images_e/219.gif) )は、全般臨床症状の評価指標であるCDR-SB(Clinical Dementia Rating Sum of Boxes)評価において18カ月時点の臨床症状の悪化をプラセボと比較して27%抑制しました。しかし、サブグループ解析のデータでは、64歳以下では6%の抑制効果でした。
)は、全般臨床症状の評価指標であるCDR-SB(Clinical Dementia Rating Sum of Boxes)評価において18カ月時点の臨床症状の悪化をプラセボと比較して27%抑制しました。しかし、サブグループ解析のデータでは、64歳以下では6%の抑制効果でした。
65歳未満のレカネマブの効果「Percent Slowing:6%」も踏まえて、外来診療場面における若年性アルツハイマー(疑い)の方からの質問を想定して、説明内容をQ&A形式でまとめてみました。
https://drive.google.com/file/d/1GIWFRmpFvN-wrNVTOupUIUhcJ4d5ZM1n/view
レカネマブ(レケンビ![[レジスタードトレードマーク]](https://blog.ss-blog.jp/_images_e/219.gif) )による治療を開始するかどうか迷った際に読むための資料として参考になれば幸いです。
)による治療を開始するかどうか迷った際に読むための資料として参考になれば幸いです。
9-21EFBC89.JPG)
Percent Slowing of Decline (%)
65歳未満:6%(CDR-SB:-0.08)
65-74歳 :23%(CDR-SB:-0.37)
75歳以上:40%(CDR-SB:-0.72)
※私の感想:
この%の持つ意味については、日本経済新聞の解説がわかりやすいです。
「不治の病」に希望の光【2023 年1月 22 日付日本経済新聞・総合5】
https://www.nikkei.com/article/DGXZQODK124WL0S3A110C2000000/
=「当初、プラセボ(偽薬)と比べて 20%あれば合格といわれていた進行抑制効果で 27%の結果を出した。」
最も効果を発揮して欲しい若年層(65歳未満)での効果が乏しいようです。
この点について高名な吉山容正先生が専門誌において解説されておりますのでご参照下さい。
実臨床におけるアルツハイマー病疾患修飾薬導入の課題─レカネマブを中心に
患者選択
レカネマブのサブグループ解析のデータ4)では75歳以上,65~75歳,65歳未満の3群のCDR-SBの結果をみると,年齢と逆相関するような形で65歳以下に対する効果が乏しい傾向がみられる.さらにMCIと軽度認知症の効果の比較においても,MCIの方で効果が乏しい傾向がある.これらのサブグループの解析の解釈には症例数の問題もあり制限があるが,本剤の進行抑制効果が最も期待されるごく軽症の若年例がレカネマブのよい治療対象グループであるかは今後のデー夕の蓄積が必要である.
より高齢者においても有効であるが,進行予防という性質上,超高齢者や身体機能低下が目立つ患者,合併症が生活機能に大きな影響を与えている患者への投与に関しては,その適性を十分検討する必要がある.
【吉山容正:実臨床におけるアルツハイマー病疾患修飾薬導入の課題─レカネマブを中心に. 医学のあゆみ Vol.287 No.13 2023年12月30日号 1047-1052 2023】
4)https://www.nejm.org/doi/full/10.1056/NEJMoa2212948
付録(Supplementary Appendix)のPDF19頁
https://www.nejm.org/doi/suppl/10.1056/NEJMoa2212948/suppl_file/nejmoa2212948_appendix.pdf
※レカネマブによる有害事象であるアミロイド関連画像異常(amyloid-related imaging abnormalities:ARIA)の発生頻度(APOEε4別の頻度)【上記NEJMより抜粋】
ARIA-E(edema/effusion):浮腫や滲出液貯留=12.6%
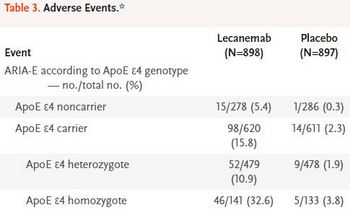
ARIA-H(hemorrhage):微小出血や脳表ヘモジデリン沈着=17.3%
レカネマブ(レケンビ
65歳未満のレカネマブの効果「Percent Slowing:6%」も踏まえて、外来診療場面における若年性アルツハイマー(疑い)の方からの質問を想定して、説明内容をQ&A形式でまとめてみました。
https://drive.google.com/file/d/1GIWFRmpFvN-wrNVTOupUIUhcJ4d5ZM1n/view
レカネマブ(レケンビ
Percent Slowing of Decline (%)
65歳未満:6%(CDR-SB:-0.08)
65-74歳 :23%(CDR-SB:-0.37)
75歳以上:40%(CDR-SB:-0.72)
※私の感想:
この%の持つ意味については、日本経済新聞の解説がわかりやすいです。
「不治の病」に希望の光【2023 年1月 22 日付日本経済新聞・総合5】
https://www.nikkei.com/article/DGXZQODK124WL0S3A110C2000000/
=「当初、プラセボ(偽薬)と比べて 20%あれば合格といわれていた進行抑制効果で 27%の結果を出した。」
最も効果を発揮して欲しい若年層(65歳未満)での効果が乏しいようです。
この点について高名な吉山容正先生が専門誌において解説されておりますのでご参照下さい。
実臨床におけるアルツハイマー病疾患修飾薬導入の課題─レカネマブを中心に
患者選択
レカネマブのサブグループ解析のデータ4)では75歳以上,65~75歳,65歳未満の3群のCDR-SBの結果をみると,年齢と逆相関するような形で65歳以下に対する効果が乏しい傾向がみられる.さらにMCIと軽度認知症の効果の比較においても,MCIの方で効果が乏しい傾向がある.これらのサブグループの解析の解釈には症例数の問題もあり制限があるが,本剤の進行抑制効果が最も期待されるごく軽症の若年例がレカネマブのよい治療対象グループであるかは今後のデー夕の蓄積が必要である.
より高齢者においても有効であるが,進行予防という性質上,超高齢者や身体機能低下が目立つ患者,合併症が生活機能に大きな影響を与えている患者への投与に関しては,その適性を十分検討する必要がある.
【吉山容正:実臨床におけるアルツハイマー病疾患修飾薬導入の課題─レカネマブを中心に. 医学のあゆみ Vol.287 No.13 2023年12月30日号 1047-1052 2023】
4)https://www.nejm.org/doi/full/10.1056/NEJMoa2212948
付録(Supplementary Appendix)のPDF19頁
https://www.nejm.org/doi/suppl/10.1056/NEJMoa2212948/suppl_file/nejmoa2212948_appendix.pdf
※レカネマブによる有害事象であるアミロイド関連画像異常(amyloid-related imaging abnormalities:ARIA)の発生頻度(APOEε4別の頻度)【上記NEJMより抜粋】
ARIA-E(edema/effusion):浮腫や滲出液貯留=12.6%
ARIA-H(hemorrhage):微小出血や脳表ヘモジデリン沈着=17.3%
アルツハイマー病「根本治療薬(アデュカヌマブ)」が迎えた正念場 [アルツハイマー病]
アルツハイマー病「根本治療薬」が迎えた正念場
https://news.yahoo.co.jp/articles/ae69c12bd2d7d98320745142c1cfef421b34c35f?
世界がFDA(アメリカ食品医薬品局)による承認の可否を固唾をのんで見守っているひとつの「薬」がある。アルツハイマー病の根本治療薬「アデュカヌマブ」だ。もし、この薬が承認されれば、病気の進行自体に直接介入する初めての薬となる。
2000年代からアルツハイマー病研究を追ってきたノンフィクション作家の下山進氏の新刊『アルツハイマー征服』から、「アデュカヌマブ」にいたる開発の長い道をハイライトする。それは、ワクチンというまったく新しい発想から始まった。
■ワクチン療法の開発
アルツハイマー病の根本治療薬の開発が、ワクチンによって開けたと言うと、どういうことなのか目を丸くする人は多いだろう。
新型コロナウイルスのワクチンをみてもわかるように、ワクチンは弱毒化した病原体を人体に注射することで生まれる抗体を利用した予防法である。抗体ができると新たな病原体が侵入してきてもそれとくっつき、無毒化する。
アルツハイマー病は、アロイス・アルツハイマーというドイツの医者が100年以上前に発見したときから、老人斑と呼ばれる神経細胞の外にできるシミと、神経細胞内にできる神経原線維変化という糸くずのような固まりを病変とすることが知られていた。これらができると、神経細胞が死に、認知症とよばれる症状が出てくるのである。
老人斑は、アミロイドβとよばれるタンパク質が固まってできたものだが、まずこれができて、次に神経原線維変化が出てくる。アミロイドβ─老人斑─神経原線維変化─神経細胞死という一連の流れ。
そのドミノの最初の1枚を抜いてしまうと考えた天才科学者がいた。デール・シェンクというサンフランシスコにある医療ベンチャーのリード・サイエンティストだ。
デール・シェンクは、アミロイドβが、原因なのであれば、そのアミロイドβをワクチンとして注射してしまえばいいと考えたのだ。それで人体に抗体が生まれれば、アルツハイマー病は治るのではないか?
当時、その医療ベンチャーだけが持っていたアルツハイマー病の症状を呈するトランス・ジェニックマウスを使って、実験をしてみた。
そうすると、老人斑はマウスの脳からきれいさっぱりと消えたのだった。それが、1999年7月8日号の『ネイチャー』に発表されると科学界のみならずジャーナリズムを巻き込んだ大騒ぎになった。
ほかの科学者が相次いで、ワクチンを注射したトランス・ジェニックマウスで、迷路を使った実験をする。すると、認知機能の低下も抑えられるという実験結果まで得られたのだった。
2000年代の初頭、アルツハイマー病は治る病気になる、と世界は沸き立った。
■AN1792の失敗から
デール・シェンクらが開発したワクチンAN1792の治験はアメリカで行ったフェーズ1を通過し、欧州にまで広げたフェーズ2に進む。
が、ここで急性髄膜脳炎という深刻な副作用が、治験を行った各病院から報告されたのである。症状は、頭痛や発熱、吐き気、患者によっては錯乱を起こし、昏睡状態に陥る患者もいた。
半身が一時的に不随になる患者や、失語症に陥る患者もいた。
ワクチンは免疫反応を強く出すために、アジュバントという物質をつけるのだが、それで自らの脳細胞を攻撃してしまうということが起こったらしい。一種の自己免疫疾患だ。治験を行っていたエラン社はAN1792の開発を中止する。
AN1792の治験を行ったサイトのひとつにチューリッヒ大学医学部があった。ここでも、30人の患者のうち3人の患者が急性髄膜脳炎を発症したが、ロジャー・ニッチ、クリストフ・ホックはこの治験に入った30人の患者をその後1年経過を観察し、追跡調査をするのである。
すると、意外なことがわかった。インフルエンザの予防接種をみてもわかるように、予防接種をしても免疫がつかない、つまり抗体が生まれない人がいる。AN1792の場合もそうだったが、この抗体が生じなかった10人は、その後急速に認知症の症状が悪化した。しかし、抗体が生じた20人の患者は、その後も認知機能の衰えがほとんど進まなかった。
ここから、ワクチンではなく、抗体そのものを投与するという発想が生まれるである。
そのころ、ほかの学者が、アルツハイマー病になりにくい人は、アミロイドβにたいする自然抗体をもともともっていることを示唆する論文を発表していた。ロジャー・ニッチとクリストフ・ホックは、大学の付属病院に保管してある1000以上の検体から、老齢になってもアルツハイマー病にならなかった人を選んで調べていき、ある抗体を発見する。
それが、後の「アデュカヌマブ」なのである。
■バイオジェン、乾坤一擲(けんこんいってき)の賭け
アメリカのボストンにある製薬会社バイオジェンには「ドラッグハンター」と呼ばれる男がいた。小さな医療ベンチャーの開発している薬に目を配り、有望なものがあると、その権利を買い上げ、大規模な治験を行うのである。
この「ドラッグハンター」アルフレッド・サンドロックとチューリッヒ大学のロジャー・ニッチは1990年代、ボストンのハーバード・メディカル・スクールで同じ師についていた同門だった。そのことから、サンドロックは、ニッチとコンタクトをとり、ニッチの発見した「自然抗体」の開発の権利を買い取る。
「アデュカヌマブ」と名付けられたその自然抗体は、バイオジェンが2012年10月から行ったフェーズ2で、認知の面で初めて評価項目を達成した薬となった。
そしてフェーズ3。
アルツハイマー病の治験は莫大な費用かかかるようになっていた。というのは、それまでのほかの薬の治験が失敗したのは、患者を適切に選んでいなかったためと考えられたからだった。PET(陽電子放出断層撮影)によってアミロイドがたまった患者、本当のアルツハイマー病の患者、しかも初期の患者を選ぶ設計の治験が必要となっていた。PETは2002年に開発された技術だが、高額の費用がかかる。
その費用は、探索研究から臨床までを含めて1薬当たり2000億から3000億円かかるようになっていた。
AN1792の治験に失敗したエラン社は失敗の痛手から経営が悪化、他社に買収され2013年に消滅してしまっていた。業界第2位のファイザーは、アルツハイマー病の薬の成功率があまりに低いこと(2002年以来、承認されている薬はない)から、神経疾患分野の創薬からは撤退することを2018年に表明していた。
それほどアルツハイマー病の創薬はリスクの高い事業だったのである。
「アデュカヌマブ」のフェーズ3はEMERGEとENGAGEという被験者総数3210名のふたつの治験が並行して行われたが、共同開発に手をあげたのが、日本の製薬会社エーザイだった。エーザイは1990年代に対症療法的な薬だが、抗認知症薬の「アリセプト」を開発し、一時はこの一薬だけで、年間3000億円以上の売り上げをあげていた。しかし、その「アリセプト」の特許も切れ、特許の崖と言われる売り上げ減に苦しんでいた。
2社ともに、社運をかけた開発だ。アルツハイマー病の患者は全世界で5000万人。日本でも400万人いる。もし「承認」されれば、リスクを回収し、莫大な売り上げとなる。
■矛盾する治験結果
さて、そのフェーズ3の治験結果が2019年末までに出たが、これが物議をかもしている。1500人以上の被験者数があるふたつの治験があい矛盾する結果になったのだ。EMERGEでは認知機能を含むすべての評価項目を達成したものの、ENGAGEでは、プラセボより悪くなったグループもある、というものだった。
バイオジェンの主張は、0、1、3、5、10ミリグラム投与の各グループで、高容量のものだけをみれば、ENGAGEでも結果は出ている、というもの。
これをもとにFDAと折衝を続け2020年7月、ついに新薬申請にこぎつけた。以来、バイオジェンとエーザイの株価は乱高下している。
FDAが11月に開いた外部の有識者からのアドバイスを求める「諮問委員会」で、サイト上に事前にFDAのペーパーがアップされると、バイオジェンの株価は45パーセントも上昇した。その文書でFDAは、バイオジェンの治験の結果は「明白なものであり、説得力がある」としていたのだ。翌日開けた東京市場でエーザイの株価はストップ高となった。
しかし、11月6日にオンラインで開かれた「諮問委員会」の評決で、11人の委員のうち委員長1人しか、承認を推薦するという投票をしなかったことがわかると、株価は暴落。
「諮問委員会」の評決にFDAは縛られるものではないが、「諮問委員会」をはずみにして一気に承認にもっていこうとしたFDAのもくろみは外れたのだった。
■矛盾する2つの治験結果に対してFDAの判定は
治験のデータが完全でないのは明白だ。矛盾する2つの治験結果がある。ではもう一度治験をすることをFDAは勧告するのか? となるとあと4年はかかる。そもそももう1本の治験をするだけの体力がバイオジェンとエーザイにあるか?
大きな影響力を持つ研究者や介護者の団体アルツハイマー協会が、「諮問委員会」のドケットによせた意見書にはこうある。
<データが不完全だという科学コミュニティの議論はわかります。しかし治療法のない現在、可能性のある治療法へのアクセスが断たれるということは、何百万人もの患者、その配偶者、母親、父親、祖父、祖母、おじ、おば、友人たち、地域の人たちにとって、とりかえしのつかないことなのです。そうした比較衡量のうえで、われわれは、この薬の「承認」を求めます>
FDAへの申請に続き、10月21日に欧州薬品庁、12月10日には日本の厚生労働省にも「アデュカヌマブ」の承認申請が、バイオジェンとエーザイによってなされた。
FDAによる運命の判定は、2021年3月7日までに下されることになっている。
【東洋経済オンライン 2021年1月11日 9:01配信 下山 進 :ノンフィクション作家】
https://news.yahoo.co.jp/articles/ae69c12bd2d7d98320745142c1cfef421b34c35f?
世界がFDA(アメリカ食品医薬品局)による承認の可否を固唾をのんで見守っているひとつの「薬」がある。アルツハイマー病の根本治療薬「アデュカヌマブ」だ。もし、この薬が承認されれば、病気の進行自体に直接介入する初めての薬となる。
2000年代からアルツハイマー病研究を追ってきたノンフィクション作家の下山進氏の新刊『アルツハイマー征服』から、「アデュカヌマブ」にいたる開発の長い道をハイライトする。それは、ワクチンというまったく新しい発想から始まった。
■ワクチン療法の開発
アルツハイマー病の根本治療薬の開発が、ワクチンによって開けたと言うと、どういうことなのか目を丸くする人は多いだろう。
新型コロナウイルスのワクチンをみてもわかるように、ワクチンは弱毒化した病原体を人体に注射することで生まれる抗体を利用した予防法である。抗体ができると新たな病原体が侵入してきてもそれとくっつき、無毒化する。
アルツハイマー病は、アロイス・アルツハイマーというドイツの医者が100年以上前に発見したときから、老人斑と呼ばれる神経細胞の外にできるシミと、神経細胞内にできる神経原線維変化という糸くずのような固まりを病変とすることが知られていた。これらができると、神経細胞が死に、認知症とよばれる症状が出てくるのである。
老人斑は、アミロイドβとよばれるタンパク質が固まってできたものだが、まずこれができて、次に神経原線維変化が出てくる。アミロイドβ─老人斑─神経原線維変化─神経細胞死という一連の流れ。
そのドミノの最初の1枚を抜いてしまうと考えた天才科学者がいた。デール・シェンクというサンフランシスコにある医療ベンチャーのリード・サイエンティストだ。
デール・シェンクは、アミロイドβが、原因なのであれば、そのアミロイドβをワクチンとして注射してしまえばいいと考えたのだ。それで人体に抗体が生まれれば、アルツハイマー病は治るのではないか?
当時、その医療ベンチャーだけが持っていたアルツハイマー病の症状を呈するトランス・ジェニックマウスを使って、実験をしてみた。
そうすると、老人斑はマウスの脳からきれいさっぱりと消えたのだった。それが、1999年7月8日号の『ネイチャー』に発表されると科学界のみならずジャーナリズムを巻き込んだ大騒ぎになった。
ほかの科学者が相次いで、ワクチンを注射したトランス・ジェニックマウスで、迷路を使った実験をする。すると、認知機能の低下も抑えられるという実験結果まで得られたのだった。
2000年代の初頭、アルツハイマー病は治る病気になる、と世界は沸き立った。
■AN1792の失敗から
デール・シェンクらが開発したワクチンAN1792の治験はアメリカで行ったフェーズ1を通過し、欧州にまで広げたフェーズ2に進む。
が、ここで急性髄膜脳炎という深刻な副作用が、治験を行った各病院から報告されたのである。症状は、頭痛や発熱、吐き気、患者によっては錯乱を起こし、昏睡状態に陥る患者もいた。
半身が一時的に不随になる患者や、失語症に陥る患者もいた。
ワクチンは免疫反応を強く出すために、アジュバントという物質をつけるのだが、それで自らの脳細胞を攻撃してしまうということが起こったらしい。一種の自己免疫疾患だ。治験を行っていたエラン社はAN1792の開発を中止する。
AN1792の治験を行ったサイトのひとつにチューリッヒ大学医学部があった。ここでも、30人の患者のうち3人の患者が急性髄膜脳炎を発症したが、ロジャー・ニッチ、クリストフ・ホックはこの治験に入った30人の患者をその後1年経過を観察し、追跡調査をするのである。
すると、意外なことがわかった。インフルエンザの予防接種をみてもわかるように、予防接種をしても免疫がつかない、つまり抗体が生まれない人がいる。AN1792の場合もそうだったが、この抗体が生じなかった10人は、その後急速に認知症の症状が悪化した。しかし、抗体が生じた20人の患者は、その後も認知機能の衰えがほとんど進まなかった。
ここから、ワクチンではなく、抗体そのものを投与するという発想が生まれるである。
そのころ、ほかの学者が、アルツハイマー病になりにくい人は、アミロイドβにたいする自然抗体をもともともっていることを示唆する論文を発表していた。ロジャー・ニッチとクリストフ・ホックは、大学の付属病院に保管してある1000以上の検体から、老齢になってもアルツハイマー病にならなかった人を選んで調べていき、ある抗体を発見する。
それが、後の「アデュカヌマブ」なのである。
■バイオジェン、乾坤一擲(けんこんいってき)の賭け
アメリカのボストンにある製薬会社バイオジェンには「ドラッグハンター」と呼ばれる男がいた。小さな医療ベンチャーの開発している薬に目を配り、有望なものがあると、その権利を買い上げ、大規模な治験を行うのである。
この「ドラッグハンター」アルフレッド・サンドロックとチューリッヒ大学のロジャー・ニッチは1990年代、ボストンのハーバード・メディカル・スクールで同じ師についていた同門だった。そのことから、サンドロックは、ニッチとコンタクトをとり、ニッチの発見した「自然抗体」の開発の権利を買い取る。
「アデュカヌマブ」と名付けられたその自然抗体は、バイオジェンが2012年10月から行ったフェーズ2で、認知の面で初めて評価項目を達成した薬となった。
そしてフェーズ3。
アルツハイマー病の治験は莫大な費用かかかるようになっていた。というのは、それまでのほかの薬の治験が失敗したのは、患者を適切に選んでいなかったためと考えられたからだった。PET(陽電子放出断層撮影)によってアミロイドがたまった患者、本当のアルツハイマー病の患者、しかも初期の患者を選ぶ設計の治験が必要となっていた。PETは2002年に開発された技術だが、高額の費用がかかる。
その費用は、探索研究から臨床までを含めて1薬当たり2000億から3000億円かかるようになっていた。
AN1792の治験に失敗したエラン社は失敗の痛手から経営が悪化、他社に買収され2013年に消滅してしまっていた。業界第2位のファイザーは、アルツハイマー病の薬の成功率があまりに低いこと(2002年以来、承認されている薬はない)から、神経疾患分野の創薬からは撤退することを2018年に表明していた。
それほどアルツハイマー病の創薬はリスクの高い事業だったのである。
「アデュカヌマブ」のフェーズ3はEMERGEとENGAGEという被験者総数3210名のふたつの治験が並行して行われたが、共同開発に手をあげたのが、日本の製薬会社エーザイだった。エーザイは1990年代に対症療法的な薬だが、抗認知症薬の「アリセプト」を開発し、一時はこの一薬だけで、年間3000億円以上の売り上げをあげていた。しかし、その「アリセプト」の特許も切れ、特許の崖と言われる売り上げ減に苦しんでいた。
2社ともに、社運をかけた開発だ。アルツハイマー病の患者は全世界で5000万人。日本でも400万人いる。もし「承認」されれば、リスクを回収し、莫大な売り上げとなる。
■矛盾する治験結果
さて、そのフェーズ3の治験結果が2019年末までに出たが、これが物議をかもしている。1500人以上の被験者数があるふたつの治験があい矛盾する結果になったのだ。EMERGEでは認知機能を含むすべての評価項目を達成したものの、ENGAGEでは、プラセボより悪くなったグループもある、というものだった。
バイオジェンの主張は、0、1、3、5、10ミリグラム投与の各グループで、高容量のものだけをみれば、ENGAGEでも結果は出ている、というもの。
これをもとにFDAと折衝を続け2020年7月、ついに新薬申請にこぎつけた。以来、バイオジェンとエーザイの株価は乱高下している。
FDAが11月に開いた外部の有識者からのアドバイスを求める「諮問委員会」で、サイト上に事前にFDAのペーパーがアップされると、バイオジェンの株価は45パーセントも上昇した。その文書でFDAは、バイオジェンの治験の結果は「明白なものであり、説得力がある」としていたのだ。翌日開けた東京市場でエーザイの株価はストップ高となった。
しかし、11月6日にオンラインで開かれた「諮問委員会」の評決で、11人の委員のうち委員長1人しか、承認を推薦するという投票をしなかったことがわかると、株価は暴落。
「諮問委員会」の評決にFDAは縛られるものではないが、「諮問委員会」をはずみにして一気に承認にもっていこうとしたFDAのもくろみは外れたのだった。
■矛盾する2つの治験結果に対してFDAの判定は
治験のデータが完全でないのは明白だ。矛盾する2つの治験結果がある。ではもう一度治験をすることをFDAは勧告するのか? となるとあと4年はかかる。そもそももう1本の治験をするだけの体力がバイオジェンとエーザイにあるか?
大きな影響力を持つ研究者や介護者の団体アルツハイマー協会が、「諮問委員会」のドケットによせた意見書にはこうある。
<データが不完全だという科学コミュニティの議論はわかります。しかし治療法のない現在、可能性のある治療法へのアクセスが断たれるということは、何百万人もの患者、その配偶者、母親、父親、祖父、祖母、おじ、おば、友人たち、地域の人たちにとって、とりかえしのつかないことなのです。そうした比較衡量のうえで、われわれは、この薬の「承認」を求めます>
FDAへの申請に続き、10月21日に欧州薬品庁、12月10日には日本の厚生労働省にも「アデュカヌマブ」の承認申請が、バイオジェンとエーザイによってなされた。
FDAによる運命の判定は、2021年3月7日までに下されることになっている。
【東洋経済オンライン 2021年1月11日 9:01配信 下山 進 :ノンフィクション作家】
クイズ:次のうち、Alzheimer型認知症を最も早期に診断できるのはどれか? [アルツハイマー病]
次のうち、Alzheimer型認知症を最も早期に診断できるのはどれか。 【株式会社テコム作成医師国家試験模擬試験問題より出題】
https://www.m3.com/quiz/doctor/pc/?id=mnc&portalId=mailmag&mmp=EB180213&mc.l=275078772
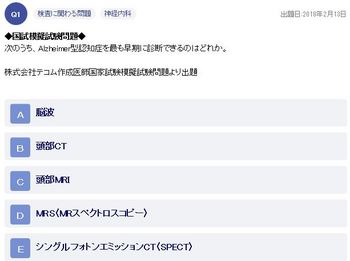
A 脳波
B 頭部CT
C 頭部MRI
D MRS〈MRスペクトロスコピー〉
E シングルフォトンエミッションCT〈SPECT〉
正解:
E シングルフォトンエミッションCT〈SPECT〉
解説:
【アプローチ】
Alzheimer型認知症の早期診断は頭頂葉、側頭葉の代謝が低下することでなされる。
【選択的考察】
A(×):非常に進行して徐波が出現するようにならないと診断できない。
B(×)、C(×):CTやMRIのような形態画像では、よほど進行してからでないと所見が得られない。
D(×):MRSは精度が低く、早期診断には適しない。
E(○):SPECTやPETのような機能画像では早期から所見が得られる。
【essential point】
CT、MRIのような形態画像で海馬の萎縮など典型的な所見が得られるのは、Alzheimer型認知症としては非常に進行した段階である。それ以前に臨床的に、あるいは機能画像で診断がついていることが普通である。
私の感想:
医師の正解率57%か・・。
脳萎縮の%に関しては、最近のデータを見かけませんので少々古いデータにはなりますが、以下に10年程前のデータをご紹介しますね。
2008年4月5日開催のアルツハイマー病研究会にて、松田博史先生が講演の中で以下のようなデータを紹介されました。

MRIにて萎縮を認める%【私の講演用スライド360】
軽度アルツハイマー病 : 25%
中等度アルツハイマー病: 40%
さて、正解はの「シングルフォトンエミッションCT〈SPECT〉」ですが、問題はその「感度&特異度」ですよね。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第411回『脳をみる検査―軽度認知障害はアルツハイマー病に進展するか?』(2014年2月20日公開)
これまでに何度も繰り返して説明しておりますように、軽度認知障害(Mild Cognitive Impairment;MCI)はアルツハイマー病(AD)の前段階として注目されている概念です。
そこで、MCIの患者さんを3年間追跡調査し、ADに進展したケースと進展しなかったケースを詳細に調べ、最初に実施したSPECT検査所見よりADへの進展が予測できるかどうかを調べる研究(J-COSMIC)が2003年より開始され、2010年3月に最終報告が発表されました。
J-COSMIC最終報告書(著者:長寿科学振興財団J-COSMIC、出版:J-COSMIC)のP25には以下のような記述があります。

「ADの予測診断能を算出したところ、感度76%、特異度39%、陽性的中率52%、陰性的中率65%であった。この結果は臨床的な認知症患者にSPECT検査を行えば80%近い確率でADが診断されるとともに、AD様所見を呈するSPECT像が認められてもADではない症例が60%以上存在することが示された。」
P.S.
J-COSMIC研究においては、軽度認知障害(Mild Cognitive Impairment;MCI)からアルツハイマー病(AD)への進展は、3年間で45.8%でした。
特異度が39%と予想外に低く、「偽陽性」が多かったことに関しては、本研究の追跡期間が3年間であったことが一因ではないかと指摘されています。すなわち、4年目以降にコンバートするケースが相当数あるため、特異度が低値になったのではないかと推察されております。いずれにせよ、SPECT検査においては「偽陽性」が多々あることは事実ですので、MCI患者さんにおいてADに特徴的な脳血流低下が確認されたとしても、それだけで安易に「将来アルツハイマー病を発症する確率が高いです」と告知することは慎まなければなりませんね。
https://www.m3.com/quiz/doctor/pc/?id=mnc&portalId=mailmag&mmp=EB180213&mc.l=275078772
A 脳波
B 頭部CT
C 頭部MRI
D MRS〈MRスペクトロスコピー〉
E シングルフォトンエミッションCT〈SPECT〉
正解:
E シングルフォトンエミッションCT〈SPECT〉
解説:
【アプローチ】
Alzheimer型認知症の早期診断は頭頂葉、側頭葉の代謝が低下することでなされる。
【選択的考察】
A(×):非常に進行して徐波が出現するようにならないと診断できない。
B(×)、C(×):CTやMRIのような形態画像では、よほど進行してからでないと所見が得られない。
D(×):MRSは精度が低く、早期診断には適しない。
E(○):SPECTやPETのような機能画像では早期から所見が得られる。
【essential point】
CT、MRIのような形態画像で海馬の萎縮など典型的な所見が得られるのは、Alzheimer型認知症としては非常に進行した段階である。それ以前に臨床的に、あるいは機能画像で診断がついていることが普通である。
私の感想:
医師の正解率57%か・・。
脳萎縮の%に関しては、最近のデータを見かけませんので少々古いデータにはなりますが、以下に10年程前のデータをご紹介しますね。
2008年4月5日開催のアルツハイマー病研究会にて、松田博史先生が講演の中で以下のようなデータを紹介されました。
MRIにて萎縮を認める%【私の講演用スライド360】
軽度アルツハイマー病 : 25%
中等度アルツハイマー病: 40%
さて、正解はの「シングルフォトンエミッションCT〈SPECT〉」ですが、問題はその「感度&特異度」ですよね。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第411回『脳をみる検査―軽度認知障害はアルツハイマー病に進展するか?』(2014年2月20日公開)
これまでに何度も繰り返して説明しておりますように、軽度認知障害(Mild Cognitive Impairment;MCI)はアルツハイマー病(AD)の前段階として注目されている概念です。
そこで、MCIの患者さんを3年間追跡調査し、ADに進展したケースと進展しなかったケースを詳細に調べ、最初に実施したSPECT検査所見よりADへの進展が予測できるかどうかを調べる研究(J-COSMIC)が2003年より開始され、2010年3月に最終報告が発表されました。
J-COSMIC最終報告書(著者:長寿科学振興財団J-COSMIC、出版:J-COSMIC)のP25には以下のような記述があります。

「ADの予測診断能を算出したところ、感度76%、特異度39%、陽性的中率52%、陰性的中率65%であった。この結果は臨床的な認知症患者にSPECT検査を行えば80%近い確率でADが診断されるとともに、AD様所見を呈するSPECT像が認められてもADではない症例が60%以上存在することが示された。」
P.S.
J-COSMIC研究においては、軽度認知障害(Mild Cognitive Impairment;MCI)からアルツハイマー病(AD)への進展は、3年間で45.8%でした。
特異度が39%と予想外に低く、「偽陽性」が多かったことに関しては、本研究の追跡期間が3年間であったことが一因ではないかと指摘されています。すなわち、4年目以降にコンバートするケースが相当数あるため、特異度が低値になったのではないかと推察されております。いずれにせよ、SPECT検査においては「偽陽性」が多々あることは事実ですので、MCI患者さんにおいてADに特徴的な脳血流低下が確認されたとしても、それだけで安易に「将来アルツハイマー病を発症する確率が高いです」と告知することは慎まなければなりませんね。
繰り返す質問(Repetitive questioning;Godot症候群) [アルツハイマー病]
認知症、ケンカの理由~異なる事実~
https://yomidr.yomiuri.co.jp/article/20160916-OYTET50014/?catname=column_kinoshita%3Ffrom%3Dfb
「おそらく、二通りの解決方法があります。ただし、効率的な選択肢ではありません。
その1.まず、なぜその事実争いが起きたのか。なぜ、泰子さんが何度も曜日を夫に尋ねるのか、に着目します。
おそらく、いつも曜日を気にするということは、なにか曜日にちなんだ用事が泰子さんの生活のリズムを作っている可能性があります。遅刻できないし、うっかり休むこともできない。聞いてみると、やはり趣味のサークルが週2回月、木曜日にある、といいます。緊張と楽しみが折り重なった気持ちなのでしょう。泰子さんには大切なイベント。今日の曜日がわからないと、不安になるのも当たり前です。別の手段で、大きな日付と曜日付き電子時計が部屋の真ん中にあれば、夫に繰り返し曜日を繰り返し尋ねることはなくなります。洞察が正しければ。」
繰り返す質問(Repetitive questioning;Godot症候群)
繰り返す質問(Repetitive questioning;Godot症候群)への対応に関してはアピタルにおいても二度ほどご紹介したことがあります。
不安への対応が基本となりますね。
それと、認知症の人は「今」この時を刹那に生きているので、「先の話をすることは絶対に控えること!」という留意点でしょうか。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第191回『認知症と長寿社会(笑顔のままで)─介護者の介護負担をどうみるか』(2013年7月9日公開)
2011年1月30日付朝日新聞朝刊の「読書」欄において、信濃毎日新聞取材班が77回にわたって連載したルポルタージュをまとめた一冊『認知症と長寿社会─笑顔のままで』(講談社現代新書)が紹介されました。
「介護者の介護負担」を評価するには、数字化しないと客観的に比較できないため、学術的にはZaritなどの指標(メモ1参照)が用いられます。しかし、現場で起きている介護者の苦悩を正確に捉えることはなかなか困難です。信濃毎日新聞取材班のルポ記事は、その捉えにくい部分を見事に表現しています。
メモ1:介護者の介護負担を評価する尺度
認知症患者さんの介護者の介護負担を評価する尺度としては、ZaritらによるZarit Caregiver Burden Interview(ZBI)が代表的な指標です。
原法は29項目の質問から構成されています。神戸学院大学大学院人文学部人間心理学科の博野信次教授(神経内科医)らは22項目からなる日本語短縮版を作成し、日本語版ZBIが介護者のburden(負担)の評価に有用であったことを報告しています。
22項目の質問に関して、介護者の反応が5段階(0~4点)で評価され、点数が高いほど負担感が強いということになります。
今までの研究では、妄想・幻覚、不安・うつ、攻撃的行動がburdenに深く関連し、見当識障害、記憶障害は関連しないことなどが報告されています(博野信次:痴呆症患者の介護者の負担─日本語版ZBIによる検討─ 脳神経 Vol.50 561-567 1998)。
なお、不安を基盤として強迫症状が出現することもあります。そのことを非常に興味深く紹介している記述がありますので以下にご紹介しましょう(一部改変)。
「アルツハイマー病(AD)における精神症状・行動異常の中で頻度が高いのは、抑うつとアパシーだが、その次に多いのが不安である。
認知症に伴う不安症状の現れ方はさまざまであり、パニック障害、身体表現性障害(心気症など)は、臨床場面においてしばしば遭遇する。その他に、予定が入っていることを何度も繰り返して聞く『Godot症候群』や、独りで残されたときに何度も電話をかけて家人を困らせるような状態もよくみられる。これらの状態は家人の介護困難感を増大させる大きな要因となりうる。軽度認知障害レベルの症例でGodot症候群を伴うと、ADへの移行率が高いとの報告がある。一方で、このような不安症状は、認知機能が中等度以上に低下するにつれて次第に軽減ないし、消退していくようである。」(編集/朝田 隆 著者/服部英幸:誤診症例から学ぶ 認知症とその他の疾患の鑑別. 医学書院, 東京, 2013, p93)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第743回『「つきまとい(シャドーイング)」への対応─作業療法もケアの一つ』(2015年1月24日公開)
さて、話題を再び「つきまとい」に戻しましょう。
独立行政法人国立長寿医療研究センターの服部英幸・行動心理療法部長は、「まとわりつき(つきまとい)の出現頻度は、軽度から中等度の認知症患者のうち67%に認められたという報告がある。不安を和らげる接し方の工夫をしたり、他の興味ある事柄(作業療法・レクリエーションなど)に参加してもらう」(服部英幸編集:BPSD初期対応ガイドライン ライフ・サイエンス, 東京, 2012, pp71-72,133)ことなどが直ちにできるケアであると報告しています。作業療法は、「つきまとい」だけではなく、繰り返す質問(Repetitive questioning;Godot症候群)にも効果があることが報告されております。
服部英幸先生は、2012年10月4日に三重県津市に講演(第9回中勢認知症集談会)に来て下さいました。
服部英幸先生が編集された著書『BPSD初期対応ガイドライン』においては、認知症の行動・心理症状(Behavioral and Psychological Symptoms of Dementia;BPSD)に関して対応方法などが具体的に紹介されております。
服部英幸先生は、著書のなかで、「行動異常」に対しては薬剤の効果が乏しいと述べております。以下にその部分をご紹介します。
「BPSDはその名の通り精神症状と行動異常の2つの状態が混在している。この2つは単独で出現することも、複数が同時に出現することもある。精神症状にはみえないものがみえる、聞こえないはずのものが聞こえる、検査で異常がみつからない身体の痛みや異常な感覚などの幻覚や、真実でないことを真実であると思い込み、説得に応じない妄想などが含まれている。そのほかにうつ気分、易怒性など気分の変調も精神症状である。一方の行動異常には徘徊、常同行為のほかに、物をあてもなく集める濫集(らんしゅう)、便をつかむ弄便などが含まれている。この2つの違いは対応にも関連している。一般に、精神症状に属するものは薬物の効果が期待できるが、行動異常では効果が乏しく、非薬物療法が中心になる。」(服部英幸:BPSD初期対応ガイドライン ライフ・サイエンス, 東京, 2012, p28)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第139回『認知症のケア 家族でもフルネームで呼んでみよう』(2013年5月13日公開)
認知症ケアアドバイザーの五島シズさん(全国高齢者ケア協会監事、認知症介護研究・研修東京センター客員上級研究員)が2013年1月10日に来津され、第10回中勢認知症集談会において、「身近な人に認知症が始まったら」というタイトルでご講演されました。
講演の中で紹介された、「好ましい接し方」というスライドは印象的な内容でした。
五島シズさんは、「好ましい接し方」として10のポイントを挙げられておりました。
1 自尊心を傷つけない
2 近づいて話す
3 情報は簡潔に伝える
4 納得のいくように話す
5 わかる言葉を話す(方言などを利用する)
6 相手の話に合わせる
7 感情に働きかける
8 フルネームで呼ぶ
9 現実を知らせる
10 昔話をする
2の「近づいて話す」に関しては、アイコンタクトは大切だが、排泄のケアをするときには、羞恥心に配慮し、目を見ないほうがよいと説明されておりました。そして、女性の排泄介助の際には、エプロンをするなどして覆ってあげると恥ずかしがらず排尿しやすくなると説明されておりました。
8の「フルネームで呼ぶ」に関連して、子どもの前で呼び合っていた「お父さん」「お母さん」という呼び方で話し掛けると、話しかけた相手が配偶者であっても、そうだと気づかないケースがあります。ところが、きちんとフルネームで呼びかけると、相手が妻だと(夫だと)分かってくれることはしばしばありますよとお話されておりました。
そして、認知症の人は「今」この時を刹那に生きているので、「先の話をすることは絶対に控えること!」とお話されました。例えば、次の日曜日に本人が会うのを楽しみに待っている娘さんが来る予定になっていた場合に、喜ばせようと思って「今度の日曜日に娘さんが来ますからね」と伝えてしまうと、急に玄関の方を気にするようになり、部屋と玄関を行き来しソワソワして落ち着かなくなってしまい認知症の行動・心理症状(Behavioral and Psychological Symptoms of Dementia;BPSD)が誘発されてしまうといったケースは実に多いですから注意して下さいねと強調されておりました。
さて皆さん、10の昔話を聞く際に、決して言ってはいけない2つの禁句があるのですがそれが何か分かりますか?
それは、「今ならこうよね」「私ならこうするわ」という反応なのです。この2つの言葉は、認知症の人が昔話に浸っている状況を現実へと連れ戻し、認知症の人が主役であるという一番重要なポイントへの配慮を欠いた発言であると五島シズさんは述べておられました。
https://yomidr.yomiuri.co.jp/article/20160916-OYTET50014/?catname=column_kinoshita%3Ffrom%3Dfb
「おそらく、二通りの解決方法があります。ただし、効率的な選択肢ではありません。
その1.まず、なぜその事実争いが起きたのか。なぜ、泰子さんが何度も曜日を夫に尋ねるのか、に着目します。
おそらく、いつも曜日を気にするということは、なにか曜日にちなんだ用事が泰子さんの生活のリズムを作っている可能性があります。遅刻できないし、うっかり休むこともできない。聞いてみると、やはり趣味のサークルが週2回月、木曜日にある、といいます。緊張と楽しみが折り重なった気持ちなのでしょう。泰子さんには大切なイベント。今日の曜日がわからないと、不安になるのも当たり前です。別の手段で、大きな日付と曜日付き電子時計が部屋の真ん中にあれば、夫に繰り返し曜日を繰り返し尋ねることはなくなります。洞察が正しければ。」
繰り返す質問(Repetitive questioning;Godot症候群)
繰り返す質問(Repetitive questioning;Godot症候群)への対応に関してはアピタルにおいても二度ほどご紹介したことがあります。
不安への対応が基本となりますね。
それと、認知症の人は「今」この時を刹那に生きているので、「先の話をすることは絶対に控えること!」という留意点でしょうか。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第191回『認知症と長寿社会(笑顔のままで)─介護者の介護負担をどうみるか』(2013年7月9日公開)
2011年1月30日付朝日新聞朝刊の「読書」欄において、信濃毎日新聞取材班が77回にわたって連載したルポルタージュをまとめた一冊『認知症と長寿社会─笑顔のままで』(講談社現代新書)が紹介されました。
「介護者の介護負担」を評価するには、数字化しないと客観的に比較できないため、学術的にはZaritなどの指標(メモ1参照)が用いられます。しかし、現場で起きている介護者の苦悩を正確に捉えることはなかなか困難です。信濃毎日新聞取材班のルポ記事は、その捉えにくい部分を見事に表現しています。
メモ1:介護者の介護負担を評価する尺度
認知症患者さんの介護者の介護負担を評価する尺度としては、ZaritらによるZarit Caregiver Burden Interview(ZBI)が代表的な指標です。
原法は29項目の質問から構成されています。神戸学院大学大学院人文学部人間心理学科の博野信次教授(神経内科医)らは22項目からなる日本語短縮版を作成し、日本語版ZBIが介護者のburden(負担)の評価に有用であったことを報告しています。
22項目の質問に関して、介護者の反応が5段階(0~4点)で評価され、点数が高いほど負担感が強いということになります。
今までの研究では、妄想・幻覚、不安・うつ、攻撃的行動がburdenに深く関連し、見当識障害、記憶障害は関連しないことなどが報告されています(博野信次:痴呆症患者の介護者の負担─日本語版ZBIによる検討─ 脳神経 Vol.50 561-567 1998)。
なお、不安を基盤として強迫症状が出現することもあります。そのことを非常に興味深く紹介している記述がありますので以下にご紹介しましょう(一部改変)。
「アルツハイマー病(AD)における精神症状・行動異常の中で頻度が高いのは、抑うつとアパシーだが、その次に多いのが不安である。
認知症に伴う不安症状の現れ方はさまざまであり、パニック障害、身体表現性障害(心気症など)は、臨床場面においてしばしば遭遇する。その他に、予定が入っていることを何度も繰り返して聞く『Godot症候群』や、独りで残されたときに何度も電話をかけて家人を困らせるような状態もよくみられる。これらの状態は家人の介護困難感を増大させる大きな要因となりうる。軽度認知障害レベルの症例でGodot症候群を伴うと、ADへの移行率が高いとの報告がある。一方で、このような不安症状は、認知機能が中等度以上に低下するにつれて次第に軽減ないし、消退していくようである。」(編集/朝田 隆 著者/服部英幸:誤診症例から学ぶ 認知症とその他の疾患の鑑別. 医学書院, 東京, 2013, p93)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第743回『「つきまとい(シャドーイング)」への対応─作業療法もケアの一つ』(2015年1月24日公開)
さて、話題を再び「つきまとい」に戻しましょう。
独立行政法人国立長寿医療研究センターの服部英幸・行動心理療法部長は、「まとわりつき(つきまとい)の出現頻度は、軽度から中等度の認知症患者のうち67%に認められたという報告がある。不安を和らげる接し方の工夫をしたり、他の興味ある事柄(作業療法・レクリエーションなど)に参加してもらう」(服部英幸編集:BPSD初期対応ガイドライン ライフ・サイエンス, 東京, 2012, pp71-72,133)ことなどが直ちにできるケアであると報告しています。作業療法は、「つきまとい」だけではなく、繰り返す質問(Repetitive questioning;Godot症候群)にも効果があることが報告されております。
服部英幸先生は、2012年10月4日に三重県津市に講演(第9回中勢認知症集談会)に来て下さいました。
服部英幸先生が編集された著書『BPSD初期対応ガイドライン』においては、認知症の行動・心理症状(Behavioral and Psychological Symptoms of Dementia;BPSD)に関して対応方法などが具体的に紹介されております。
服部英幸先生は、著書のなかで、「行動異常」に対しては薬剤の効果が乏しいと述べております。以下にその部分をご紹介します。
「BPSDはその名の通り精神症状と行動異常の2つの状態が混在している。この2つは単独で出現することも、複数が同時に出現することもある。精神症状にはみえないものがみえる、聞こえないはずのものが聞こえる、検査で異常がみつからない身体の痛みや異常な感覚などの幻覚や、真実でないことを真実であると思い込み、説得に応じない妄想などが含まれている。そのほかにうつ気分、易怒性など気分の変調も精神症状である。一方の行動異常には徘徊、常同行為のほかに、物をあてもなく集める濫集(らんしゅう)、便をつかむ弄便などが含まれている。この2つの違いは対応にも関連している。一般に、精神症状に属するものは薬物の効果が期待できるが、行動異常では効果が乏しく、非薬物療法が中心になる。」(服部英幸:BPSD初期対応ガイドライン ライフ・サイエンス, 東京, 2012, p28)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第139回『認知症のケア 家族でもフルネームで呼んでみよう』(2013年5月13日公開)
認知症ケアアドバイザーの五島シズさん(全国高齢者ケア協会監事、認知症介護研究・研修東京センター客員上級研究員)が2013年1月10日に来津され、第10回中勢認知症集談会において、「身近な人に認知症が始まったら」というタイトルでご講演されました。
講演の中で紹介された、「好ましい接し方」というスライドは印象的な内容でした。
五島シズさんは、「好ましい接し方」として10のポイントを挙げられておりました。
1 自尊心を傷つけない
2 近づいて話す
3 情報は簡潔に伝える
4 納得のいくように話す
5 わかる言葉を話す(方言などを利用する)
6 相手の話に合わせる
7 感情に働きかける
8 フルネームで呼ぶ
9 現実を知らせる
10 昔話をする
2の「近づいて話す」に関しては、アイコンタクトは大切だが、排泄のケアをするときには、羞恥心に配慮し、目を見ないほうがよいと説明されておりました。そして、女性の排泄介助の際には、エプロンをするなどして覆ってあげると恥ずかしがらず排尿しやすくなると説明されておりました。
8の「フルネームで呼ぶ」に関連して、子どもの前で呼び合っていた「お父さん」「お母さん」という呼び方で話し掛けると、話しかけた相手が配偶者であっても、そうだと気づかないケースがあります。ところが、きちんとフルネームで呼びかけると、相手が妻だと(夫だと)分かってくれることはしばしばありますよとお話されておりました。
そして、認知症の人は「今」この時を刹那に生きているので、「先の話をすることは絶対に控えること!」とお話されました。例えば、次の日曜日に本人が会うのを楽しみに待っている娘さんが来る予定になっていた場合に、喜ばせようと思って「今度の日曜日に娘さんが来ますからね」と伝えてしまうと、急に玄関の方を気にするようになり、部屋と玄関を行き来しソワソワして落ち着かなくなってしまい認知症の行動・心理症状(Behavioral and Psychological Symptoms of Dementia;BPSD)が誘発されてしまうといったケースは実に多いですから注意して下さいねと強調されておりました。
さて皆さん、10の昔話を聞く際に、決して言ってはいけない2つの禁句があるのですがそれが何か分かりますか?
それは、「今ならこうよね」「私ならこうするわ」という反応なのです。この2つの言葉は、認知症の人が昔話に浸っている状況を現実へと連れ戻し、認知症の人が主役であるという一番重要なポイントへの配慮を欠いた発言であると五島シズさんは述べておられました。
SED-11Q [アルツハイマー病]
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第31回『認知症の代表的疾患─レビー小体型認知症 もの忘れを自覚することの多いレビー小体型』(2013年1月14日公開)
もの忘れに関しても、DLBにおいては内省できることが多いことが報告されています。
アルツハイマー病では、初期ですらもの忘れを自覚していないケースが多いです。一方、DLBでは、初期においてはもの忘れを自覚しているケースが多いのです。
東京医科大学病院老年病科の羽生春夫教授は、疾患別の病識の有無について検討しており、「有意な認知機能障害を認めない老年者コントロールの病識低下度の平均+2標準偏差を超えるものを病識低下ありと定義すると、AD(アルツハイマー病)群の65%、MCI(軽度認知障害)群の34%、DLB(レビー小体型認知症)群の6%、VaD(血管性認知症)群の36%が該当し、AD群が最も多く、DLB群は最も少なかった。」(羽生春夫:老年期認知症患者の病識―生活健忘チェックリストを用い、介護者を対照とした研究―. 日本老年医学会雑誌 Vol.44 No.4 463-469 2007)と報告しております。
メモ:内省
「記憶、見当識、思考、言葉や数の抽象化機能などは、日常生活を送っていく上でそれぞれがとても大切な機能である。しかし、暮らしのなかでは、これらの機能一つひとつがバラバラに役立っているわけではない。複数の知的道具あるいは要素的知能を組み合わせて使いこなす『何か』がなけれはならないはずである。それを知的主体あるいは知的『私』とよぶことにすると、そこに障害が及ぶのである。だから、認知症を病む人は、いろいろなことができなくなるという以上に、『私が壊れる!』と正しく感じとるのである。
知的主体などという硬い言葉ではなく、もう少しうまい言葉が見つかればよいのだが、学者も苦労してこの『何か』を『内省能力』(ツット)、『本来の知能』(ヤスパース)、『知的人格』『知的スーパーバイザー』(室伏)などと名づけている。どれもが、個別の、記憶、見当識、言葉、数といった道具的、要素的知能を統括する、より上位の知的機能を何とか言い表そうと苦労しているのである。」(小澤 勲:認知症とは何か 岩波新書出版, 東京, 2005, pp141-143)
認知症の介護においては、しばしばアパシー(自発性の低下・無関心)の存在が問題となります。
アパシー(apathy)とは、無気力・無関心・無感動のため、周りがやるようにと促しても、本人は面倒だから、全然動こうとしないし気にもしない状態です。そして、このアパシーの存在ゆえに、認知症がうつ病と誤診されているケースもあります。
なお、DLBでは、うつ病を有する頻度が比較的高いことも知られております。
「Ballardら(1999)は病理診断されたDLB、AD各40例を比較し、DLBでは、初診時に幻視、幻聴、妄想、誤認妄想、うつ病を有する頻度がADに比べて高い」と報告しています(長濱康弘:レビー小体型認知症の臨床症候学と病態生理. Dementia Japan Vol.25 145-155 2011)。
なおこの点に関して筑波大学臨床医学系精神医学の朝田隆教授は、「伝統的な精神科のうつに対する見方では、悲哀感、悲しみをもって『うつ』の本質とし、それに不安ややる気のなさを加えます。DLBの場合、精神科の伝統的なうつというよりは基本的にはアパシーです。周りは困っているが本人は何もしなくて当然とケロッとしているような患者さんが比較的多いですね。」と指摘しています(朝田 隆 et al:座談会─認知症の早期発見・薬物治療・生活上の障害への対策. Geriatric Medicine Vol.50 977-985 2012)。
Facebookコメント
2014年7月30日にホテルグリーンパーク津において開催されました第16回中勢認知症集談会特別講演会には、群馬大学大学院保健学研究科リハビリテーション学講座の山口晴保教授らが講師として来て下さいました。
山口晴保先生は、「MCIとADの境界は、『病識の有無』だと思っています」と講演で述べられました。そして、SED-11Q(Symptoms of Early Dementia-11 Questionnaire)を用いた病識の評価に関する検討結果についてご紹介して下さいました。
判断基準
医療機関においてはSED-11Qが11項目中3項目以上で認知症を強く疑い、地域の認知症スクリーニングでは11項目中4項目以上で受診を勧めるというのが目安だそうです。
SED-11Q【認知症初期症状11項目質問票】
①同じことを何回も話したり、尋ねたりする
②出来事の前後関係がわからなくなった
③服装などの身の回りに無頓着になった
④水道栓やドアを閉め忘れたり、後かたづけがきちんとできなくなった
⑤同時に二つの作業を行うと、一つを忘れる
⑥薬を管理してきちんと内服することができなくなった
⑦以前はてきぱきできた家事や作業に手間取るようになった
⑧計画を立てられなくなった
⑨複雑な話を理解できない
⑩興味が薄れ、意欲がなくなり、趣味活動などを止めてしまった
⑪前よりも怒りっぽくなったり、疑い深くなった
※上記の11項目に関して、ご本人は病識が欠如しているため「該当しない」にチェックを入れるものの家族はそれを感じているため「該当する」にチェックを入れ、その差がMCIにおいては乖離しないものの、軽度AD&中等度ADにおいては有意に乖離(p<0.001)しているそうです。
そして、「その結果を介護者に見せて、本人の自覚が乏しいことを理解してもらい、叱らないように指導することでBPSDを予防しましょう」と講演会で配布されました資料には記載されておりました。
詳細は論文をご参照下さい。
Maki Y, Yamaguchi T, Yamaguchi H:Symptoms of Early Dementia-11 Questionnaire(SED-11Q): A brief informant-based screening for dementia. Dement Geriatr Cogn Disord Extra Vol.3 131-142 2013
Maki Y, Yamaguchi T, Yamaguchi H:Evaluation of Anosognosia in Alzheimer's Disease Using the Symptoms of Early Dementia-11 Questionnaire(SED-11Q). Dement Geriatr Cogn Disord Extra Vol.3 351-359 2013
P.S.
MCI段階で留まっているのかADに進展したのかを判断する基準は、「生活自立能力」の有無!
「生活自立能力」については、シリーズ第73回『軽度認知障害─軽度認知障害から認知症への進展』(http://apital.asahi.com/article/kasama/2013030600003.html)をご参照下さい。
Facebookコメント
認知症初期症状11項目質問票(SED-11Q)の評価用紙は山口晴保研究室のホームページ(http://www.orahoo.com/yamaguchi-h/)からダウンロード可能(山口晴保:認知症の本質を知り、リハビリテーションに活かす. MEDICAL REHABILITATION No.164 1-7 2013)。
Facebookコメント
「ところで、認知症の人には『自分は病気である』という自覚はあるのでしょうか?
この『自分は病気だ』と自覚することを『病識』といいます。医師の中には、認知症の人には『病識がある』という人もいれば、『ない』という人もいます。
私は『病識は低下している(一部ある)』という考えです。自分はどんな病気でどのような問題が生じているのかといった自覚は乏しくなっていますが、『何だかいつもと違う』という感覚はあると思っています。これを『病感』といいます。」(山口晴保:認知症にならない、負けない生き方 サンマーク出版, 東京, 2014, p53)
もの忘れに関しても、DLBにおいては内省できることが多いことが報告されています。
アルツハイマー病では、初期ですらもの忘れを自覚していないケースが多いです。一方、DLBでは、初期においてはもの忘れを自覚しているケースが多いのです。
東京医科大学病院老年病科の羽生春夫教授は、疾患別の病識の有無について検討しており、「有意な認知機能障害を認めない老年者コントロールの病識低下度の平均+2標準偏差を超えるものを病識低下ありと定義すると、AD(アルツハイマー病)群の65%、MCI(軽度認知障害)群の34%、DLB(レビー小体型認知症)群の6%、VaD(血管性認知症)群の36%が該当し、AD群が最も多く、DLB群は最も少なかった。」(羽生春夫:老年期認知症患者の病識―生活健忘チェックリストを用い、介護者を対照とした研究―. 日本老年医学会雑誌 Vol.44 No.4 463-469 2007)と報告しております。
メモ:内省
「記憶、見当識、思考、言葉や数の抽象化機能などは、日常生活を送っていく上でそれぞれがとても大切な機能である。しかし、暮らしのなかでは、これらの機能一つひとつがバラバラに役立っているわけではない。複数の知的道具あるいは要素的知能を組み合わせて使いこなす『何か』がなけれはならないはずである。それを知的主体あるいは知的『私』とよぶことにすると、そこに障害が及ぶのである。だから、認知症を病む人は、いろいろなことができなくなるという以上に、『私が壊れる!』と正しく感じとるのである。
知的主体などという硬い言葉ではなく、もう少しうまい言葉が見つかればよいのだが、学者も苦労してこの『何か』を『内省能力』(ツット)、『本来の知能』(ヤスパース)、『知的人格』『知的スーパーバイザー』(室伏)などと名づけている。どれもが、個別の、記憶、見当識、言葉、数といった道具的、要素的知能を統括する、より上位の知的機能を何とか言い表そうと苦労しているのである。」(小澤 勲:認知症とは何か 岩波新書出版, 東京, 2005, pp141-143)
認知症の介護においては、しばしばアパシー(自発性の低下・無関心)の存在が問題となります。
アパシー(apathy)とは、無気力・無関心・無感動のため、周りがやるようにと促しても、本人は面倒だから、全然動こうとしないし気にもしない状態です。そして、このアパシーの存在ゆえに、認知症がうつ病と誤診されているケースもあります。
なお、DLBでは、うつ病を有する頻度が比較的高いことも知られております。
「Ballardら(1999)は病理診断されたDLB、AD各40例を比較し、DLBでは、初診時に幻視、幻聴、妄想、誤認妄想、うつ病を有する頻度がADに比べて高い」と報告しています(長濱康弘:レビー小体型認知症の臨床症候学と病態生理. Dementia Japan Vol.25 145-155 2011)。
なおこの点に関して筑波大学臨床医学系精神医学の朝田隆教授は、「伝統的な精神科のうつに対する見方では、悲哀感、悲しみをもって『うつ』の本質とし、それに不安ややる気のなさを加えます。DLBの場合、精神科の伝統的なうつというよりは基本的にはアパシーです。周りは困っているが本人は何もしなくて当然とケロッとしているような患者さんが比較的多いですね。」と指摘しています(朝田 隆 et al:座談会─認知症の早期発見・薬物治療・生活上の障害への対策. Geriatric Medicine Vol.50 977-985 2012)。
Facebookコメント
2014年7月30日にホテルグリーンパーク津において開催されました第16回中勢認知症集談会特別講演会には、群馬大学大学院保健学研究科リハビリテーション学講座の山口晴保教授らが講師として来て下さいました。
山口晴保先生は、「MCIとADの境界は、『病識の有無』だと思っています」と講演で述べられました。そして、SED-11Q(Symptoms of Early Dementia-11 Questionnaire)を用いた病識の評価に関する検討結果についてご紹介して下さいました。
判断基準
医療機関においてはSED-11Qが11項目中3項目以上で認知症を強く疑い、地域の認知症スクリーニングでは11項目中4項目以上で受診を勧めるというのが目安だそうです。
SED-11Q【認知症初期症状11項目質問票】
①同じことを何回も話したり、尋ねたりする
②出来事の前後関係がわからなくなった
③服装などの身の回りに無頓着になった
④水道栓やドアを閉め忘れたり、後かたづけがきちんとできなくなった
⑤同時に二つの作業を行うと、一つを忘れる
⑥薬を管理してきちんと内服することができなくなった
⑦以前はてきぱきできた家事や作業に手間取るようになった
⑧計画を立てられなくなった
⑨複雑な話を理解できない
⑩興味が薄れ、意欲がなくなり、趣味活動などを止めてしまった
⑪前よりも怒りっぽくなったり、疑い深くなった
※上記の11項目に関して、ご本人は病識が欠如しているため「該当しない」にチェックを入れるものの家族はそれを感じているため「該当する」にチェックを入れ、その差がMCIにおいては乖離しないものの、軽度AD&中等度ADにおいては有意に乖離(p<0.001)しているそうです。
そして、「その結果を介護者に見せて、本人の自覚が乏しいことを理解してもらい、叱らないように指導することでBPSDを予防しましょう」と講演会で配布されました資料には記載されておりました。
詳細は論文をご参照下さい。
Maki Y, Yamaguchi T, Yamaguchi H:Symptoms of Early Dementia-11 Questionnaire(SED-11Q): A brief informant-based screening for dementia. Dement Geriatr Cogn Disord Extra Vol.3 131-142 2013
Maki Y, Yamaguchi T, Yamaguchi H:Evaluation of Anosognosia in Alzheimer's Disease Using the Symptoms of Early Dementia-11 Questionnaire(SED-11Q). Dement Geriatr Cogn Disord Extra Vol.3 351-359 2013
P.S.
MCI段階で留まっているのかADに進展したのかを判断する基準は、「生活自立能力」の有無!
「生活自立能力」については、シリーズ第73回『軽度認知障害─軽度認知障害から認知症への進展』(http://apital.asahi.com/article/kasama/2013030600003.html)をご参照下さい。
Facebookコメント
認知症初期症状11項目質問票(SED-11Q)の評価用紙は山口晴保研究室のホームページ(http://www.orahoo.com/yamaguchi-h/)からダウンロード可能(山口晴保:認知症の本質を知り、リハビリテーションに活かす. MEDICAL REHABILITATION No.164 1-7 2013)。
Facebookコメント
「ところで、認知症の人には『自分は病気である』という自覚はあるのでしょうか?
この『自分は病気だ』と自覚することを『病識』といいます。医師の中には、認知症の人には『病識がある』という人もいれば、『ない』という人もいます。
私は『病識は低下している(一部ある)』という考えです。自分はどんな病気でどのような問題が生じているのかといった自覚は乏しくなっていますが、『何だかいつもと違う』という感覚はあると思っています。これを『病感』といいます。」(山口晴保:認知症にならない、負けない生き方 サンマーク出版, 東京, 2014, p53)
落とし穴課題(Pitfall task) [アルツハイマー病]
3-3 落とし穴課題(Pitfall task)
1枚の画像を見せて、その画像の示す意味(状況)がわかるかどうかをチェックする課題です。
https://www.facebook.com/photo.php?fbid=617800405056309&set=a.530169687152715.1073741826.100004790640447&type=3&theater
図1-3に示すイラストを見せ、「何が起こっている?」と質問して、その全体像を捉えられるか(正解は「落とし穴」)、また「(人物を指しながら)真ん中の人は何をしている?」と質問して、登場人物の行動意図を読み取れるか(正解は「落とし穴に落ちるところを想像しながら隠れて見張っている」)という点から、認知症らしさを見抜く簡便な検査です。最初の質問で「落とし穴」と気づけたのは、健常者の65%、MCIの33%、軽度アルツハイマー型認知症の25%、中等度アルツハイマー型認知症の0%でした(文献)。中央の人物については「かくれんぼ」などと答え、右上部の人物については「バンザイ」などと答えるのが、アルツハイマー型認知症の特徴でした。
【山口晴保:紙とペンでできる認知症診療術―笑顔の生活を支えよう 協同医書出版社, 東京, 2016 pp21-22】
私の感想:
行動意図は、共感できるかどうかをチェックするテストでしょうね。
「こころの理論」を簡単にチェックしているようですね。
文献:
Yamaguchi T,Maki Y,Yamaguchi H:Pitfall Intention Explanation Task with Clue Questions(Pitfall task):assessment of comprehending other people's behavioral intentions in Alzheimer's disease.Int Psychogeriatr Vol24(12):1919-1926 2012
P.S.
社会的認知能力―人や社会との適切なかかわり
社会において適切な行動をとり、ほかの人がどのように感じているかを読み取る能力を社会的認知能力social cognitionと呼ぶ。人の表情をみてその感情を読み取る(感情の認識recognition of emotions)、人のこころの動きの一般的なルール(こころの理論theory of mind)を理解する能力である。障害されると、社会から受け入れられる範囲を超えた不適切な態度をとることになり、友人や家族の反対を無視する行動や安全を無視した決断など、社会的な基準に適さない行動がみられる。
認知症(DSM-5)では、社会から受け入れられる範囲を越えた態度をとる。衣服、政治、宗教、性的な会話などで皆に関心がない話題にこだわる、友人や家族の反対を無視する行動、安全を無視した決断(気候や社会的状況に不適切なもの)など、社会的な基準に鈍感な行動がみられる。
軽度認知障害(DSM-5)では、行動や態度の微妙な変化、しばしばパーソナリティ変化とされるもの、たとえば社会的にしてはいけないことに気づくとか、ひとの表情をみて察するとかということが障害される。また、共感が乏しくなるとか、過度に内向き、外向きとなるとかといったことが、ときどきみられる。あるいは微妙なアパシーや不穏などもみられる。
社会的認知能力は次のように評価される(DSM-5)。
●情動の認識recognition of emotions:
強い情動を示している顔の絵をみてそれを理解する。
●心の理論theory of mind:ひとのこころや経験の状況を推し量る能力。写真をみせて、このカバンをなくした女の子はどこを探したらよいか、とか、この男の子はどうして悲しんでいるのか? といった質問をする。
【三好功峰:認知症─正しい理解と診断技法 中山書店, 東京, 2014, pp35-36】
1枚の画像を見せて、その画像の示す意味(状況)がわかるかどうかをチェックする課題です。
https://www.facebook.com/photo.php?fbid=617800405056309&set=a.530169687152715.1073741826.100004790640447&type=3&theater
図1-3に示すイラストを見せ、「何が起こっている?」と質問して、その全体像を捉えられるか(正解は「落とし穴」)、また「(人物を指しながら)真ん中の人は何をしている?」と質問して、登場人物の行動意図を読み取れるか(正解は「落とし穴に落ちるところを想像しながら隠れて見張っている」)という点から、認知症らしさを見抜く簡便な検査です。最初の質問で「落とし穴」と気づけたのは、健常者の65%、MCIの33%、軽度アルツハイマー型認知症の25%、中等度アルツハイマー型認知症の0%でした(文献)。中央の人物については「かくれんぼ」などと答え、右上部の人物については「バンザイ」などと答えるのが、アルツハイマー型認知症の特徴でした。
【山口晴保:紙とペンでできる認知症診療術―笑顔の生活を支えよう 協同医書出版社, 東京, 2016 pp21-22】
私の感想:
行動意図は、共感できるかどうかをチェックするテストでしょうね。
「こころの理論」を簡単にチェックしているようですね。
文献:
Yamaguchi T,Maki Y,Yamaguchi H:Pitfall Intention Explanation Task with Clue Questions(Pitfall task):assessment of comprehending other people's behavioral intentions in Alzheimer's disease.Int Psychogeriatr Vol24(12):1919-1926 2012
P.S.
社会的認知能力―人や社会との適切なかかわり
社会において適切な行動をとり、ほかの人がどのように感じているかを読み取る能力を社会的認知能力social cognitionと呼ぶ。人の表情をみてその感情を読み取る(感情の認識recognition of emotions)、人のこころの動きの一般的なルール(こころの理論theory of mind)を理解する能力である。障害されると、社会から受け入れられる範囲を超えた不適切な態度をとることになり、友人や家族の反対を無視する行動や安全を無視した決断など、社会的な基準に適さない行動がみられる。
認知症(DSM-5)では、社会から受け入れられる範囲を越えた態度をとる。衣服、政治、宗教、性的な会話などで皆に関心がない話題にこだわる、友人や家族の反対を無視する行動、安全を無視した決断(気候や社会的状況に不適切なもの)など、社会的な基準に鈍感な行動がみられる。
軽度認知障害(DSM-5)では、行動や態度の微妙な変化、しばしばパーソナリティ変化とされるもの、たとえば社会的にしてはいけないことに気づくとか、ひとの表情をみて察するとかということが障害される。また、共感が乏しくなるとか、過度に内向き、外向きとなるとかといったことが、ときどきみられる。あるいは微妙なアパシーや不穏などもみられる。
社会的認知能力は次のように評価される(DSM-5)。
●情動の認識recognition of emotions:
強い情動を示している顔の絵をみてそれを理解する。
●心の理論theory of mind:ひとのこころや経験の状況を推し量る能力。写真をみせて、このカバンをなくした女の子はどこを探したらよいか、とか、この男の子はどうして悲しんでいるのか? といった質問をする。
【三好功峰:認知症─正しい理解と診断技法 中山書店, 東京, 2014, pp35-36】
アリセプトの休薬期間は? [アルツハイマー病]
アリセプトでまずまず維持されてます(休薬事例のご紹介)
https://www.facebook.com/photo.php?fbid=604703609699322&set=a.530169687152715.1073741826.100004790640447&type=3&theater
本日の再診患者さんです。
70歳代の女性の経過です。
当初は一人で通院されてました。一時、改訂長谷川式認知症スクリーニングテスト(HDS-R)は30点満点まで回復した事例です。
H25.12.13~H26.7.1、受診を中断されやや悪化。
アリセプトを再開し、現在はまずまず維持されています。
「よろしければ7月9日のD7にお越し下さいね」と声がけしておきました。
なお、一般的には、アリセプトは休薬するにしても「6週以内で」と指導されることが多いと思いますが、この事例のように7か月休薬してもその後回復するケースはあるようです。
朝日新聞アスパラクラブ「ひょっとして認知症-PartⅠ」第13回『増えるかな! 認知症の薬』(2010年11月26日公開)
認知症新薬の一つとして期待されていたガランタミンが承認されそうだという一報が飛び込んできました。
アルツハイマー病の治療薬は、日本では、ドネペジル(商品名:アリセプト)という薬が唯一の薬剤です。しかし、2010年には、海外で普及している3種類の治療薬(メマンチン、ガランタミン、リバスチグミン)の承認申請がありましたので、2011年には販売開始となる可能性もあります。
3種類の治療薬の特徴を簡単に述べます。
ガランタミンはアリセプトより副作用がやや少ないことが期待されております。リバスチグミンはパッチ剤ですので、服用を拒否する傾向がある認知症患者さんには使いやすいタイプとなります。メマンチンは海外では主に中等度~高度の患者さんに用いられており、また、アリセプトとの併用でも有用性が認められています。
今回は、認知症薬剤の有効率に関してお伝えしたいと思います。
2001年5月3日付朝日新聞名古屋本社版・声に、「医療を支えるわずかな望み」という題名で以下のような投書がありました。
「ドネペジルに関しては、須貝佑一先生が1999年11月24日付朝日新聞論壇で指摘しているように、過剰期待は禁物です。私は少数例ながらも著効例があることを報告しました。著効例は、わずか3%に過ぎません。しかしご家族からは、見違えるように良くなったと喜びの声が聞かれています。」
この投稿者は私です。
ドネペジルの薬効に関しては、第7回でも紹介しました。お忘れの方もおられると思いますので、少し復習しましょう。
ドネペジルの効果は、1年程度進行を遅らせることが目的であり、進行を停止できるわけではありません。1年間服用後も飲み続けたほうが進行を緩やかにできるので、副作用がなければ、長期間服用することになります。ただし、すべての人に効果があるわけではなく、3~4割程度の方に有効な薬剤です。
実は、ドネペジルの有効率はもっと高いという報告もあります。
鳥取大学生体制御学・浦上克哉先生の報告では、改善した症状に関して家族から細かく聞き取り調査をして有効率を算出すると、有効率は48%であったそうです(CLINICIAN vol.54 No.563 1122-1129 2007)。
詳しいデータをお知りになりたい方は以下をお読み下さい。
http://www.e-clinician.net/vol54/no563/pdf/sp15_563.pdf
へぇ~! そうなんだ! 検討方法が違うと有効率も違ってくるんだ! 有効率だけ見ていてもダメなんですね?!
そう! だから医療情報を判断することは難しいんだ!
笠間先生の「著効」ってどんな方なんですか?
私は、投薬開始3か月時点で、改訂長谷川式簡易知能評価スケール(HDS-R)が4点以上改善した症例を有効例として、HDS-Rの点数の改善に加えてご家族の印象としても著しく改善した場合を「著効例」としています。
ドネペジルが非常によく効く方というのは、いったいどのような経過を辿るのか、簡単にご紹介します。
81歳の女性は、1995年より認知症の症状が出現しました。1999年には家族の顔さえも分からなくなっていました。物盗られ妄想・徘徊・尿失禁なども出現し、2000年11月1日初めて私の外来を受診されました。初診時の改訂長谷川式簡易知能評価スケール(HDS-R)は30点満点中の10点でした。
ご存じのように、介護保険制度は2000年4月に制度開始になりました。この方は制度が始まってまもなく認定されており、要介護判定は5段階中4番目に重い要介護4でした。
ドネペジル開始後、話が理解できるようになったと家族より喜びの声が聞かれ、また徘徊も消失しました。投薬開始後3か月目のHDS-Rは、15点まで改善していました。しかし、2001年9月に、ご家族の体調不良で通院困難となり、家族の判断でドネペジルを中断したところ、症状はいっきに悪化しHDS-Rは8点まで低下しました。
講演会やメール相談で、時折質問を受けることの一つに、「アリセプトはいつまで続けるのでしょうか?」という質問があります。
この質問に対しては、私は次のように回答しております。
「ドネペジルは、認知機能の低下を3~5年間抑制し続けると考えられています。可能でしたら服薬を継続した方が良いと思います。しかし、継続が困難でしたら一度中断してみて、症状の悪化がないことを確認すれば、中止を検討されても良いと思います。」
えっ?! いったん開始した認知症薬剤が中止できることもあるの?
はい! 手術などで薬が服用できず、中止せざるを得ない場合もありますからね!
でも紹介したケースのように、中止するといっきに症状が悪化するケースもありますから、素人判断で中止することはやめて下さいね。
では、再開するのであればいつまでに再開すれば問題ないのでしょうか。
この点に関して、金沢大学大学院医学系研究科脳老化・神経病態学(神経内科)の山田正仁教授は、「6週以上の休薬では進行抑制効果そのものが消失する可能性がある」と指摘しています(日本医事新報 No.4410 69-73 2008)。最近では、可能であれば休薬期間は3週間以内にとどめるべきという意見もありますので、その辺りを目安に判断して下さいね。
アルツハイマー病は確かに不治の病です。しかし、私自身この3%という数字には支えられています。高齢だからと簡単に諦めずに、治療の道を模索して下さいね。
メモ: 改訂長谷川式認知症スクリーニングテスト(HDS-R)
HDS-Rは、認知症のスクリーニングテストとしてわが国で開発されたもので30点満点です。
通院介助のヘルパー
投稿者:梨木 投稿日時:10/11/26 17:58
著効のあった方がヘルパーと通院・服薬出来ていれば、ご本人様はもとよりご家族の介護負担も軽減されたのでは、と残念に思いました。
その後、介護保険の改定で、医療機関内での付き添いに原則介護ヘルパーは認められなくなりましたが、ヘルパーが一旦帰って又お迎えに行くのも現実的でなく、私の勤務先では、その間自費ヘルパーだけれども割引料金で設定していました。
ただ、利用者様が医師の説明を理解できない強度の難聴・認知症の場合、その理由を主治医様から書面で証明して頂いて、介護保険で対応できた例もありました。自治体で違うでしょうが。
今後介護保険もどんどん制限が増え、創設の理念から離れて行くように見えます。
目の前の支出を少し抑えることで、かえって将来のQOLの低下、介護負担増、医療費増などに結びつくのではと心配しています。
Re:通院介助のヘルパー
投稿者:笠間 睦 投稿日時:10/11/26 22:05
梨木さんへ
この方は、遠方から通院されていた方でした。
通院を中断する前に、私の方に連絡して頂ければ良かったのですが・・。
幸いこの患者さんの場合、その後介護者の方の体調が戻り、比較的早い時期に内服を再開できましたので、服薬中止前の状態に近い状況まで回復することが可能でした。
コメントありがとうございました。
Re:Re:通院介助のヘルパー
投稿者:梨木 投稿日時:10/11/28 10:36
良かったですね。
ご家族様の状況が変わった時、ケアマネジャーや地域包括センターにご相談いただくと、手段があることをお伝えしたく書きました。
https://www.facebook.com/photo.php?fbid=604703609699322&set=a.530169687152715.1073741826.100004790640447&type=3&theater
本日の再診患者さんです。
70歳代の女性の経過です。
当初は一人で通院されてました。一時、改訂長谷川式認知症スクリーニングテスト(HDS-R)は30点満点まで回復した事例です。
H25.12.13~H26.7.1、受診を中断されやや悪化。
アリセプトを再開し、現在はまずまず維持されています。
「よろしければ7月9日のD7にお越し下さいね」と声がけしておきました。
なお、一般的には、アリセプトは休薬するにしても「6週以内で」と指導されることが多いと思いますが、この事例のように7か月休薬してもその後回復するケースはあるようです。
朝日新聞アスパラクラブ「ひょっとして認知症-PartⅠ」第13回『増えるかな! 認知症の薬』(2010年11月26日公開)
認知症新薬の一つとして期待されていたガランタミンが承認されそうだという一報が飛び込んできました。
アルツハイマー病の治療薬は、日本では、ドネペジル(商品名:アリセプト)という薬が唯一の薬剤です。しかし、2010年には、海外で普及している3種類の治療薬(メマンチン、ガランタミン、リバスチグミン)の承認申請がありましたので、2011年には販売開始となる可能性もあります。
3種類の治療薬の特徴を簡単に述べます。
ガランタミンはアリセプトより副作用がやや少ないことが期待されております。リバスチグミンはパッチ剤ですので、服用を拒否する傾向がある認知症患者さんには使いやすいタイプとなります。メマンチンは海外では主に中等度~高度の患者さんに用いられており、また、アリセプトとの併用でも有用性が認められています。
今回は、認知症薬剤の有効率に関してお伝えしたいと思います。
2001年5月3日付朝日新聞名古屋本社版・声に、「医療を支えるわずかな望み」という題名で以下のような投書がありました。
「ドネペジルに関しては、須貝佑一先生が1999年11月24日付朝日新聞論壇で指摘しているように、過剰期待は禁物です。私は少数例ながらも著効例があることを報告しました。著効例は、わずか3%に過ぎません。しかしご家族からは、見違えるように良くなったと喜びの声が聞かれています。」
この投稿者は私です。
ドネペジルの薬効に関しては、第7回でも紹介しました。お忘れの方もおられると思いますので、少し復習しましょう。
ドネペジルの効果は、1年程度進行を遅らせることが目的であり、進行を停止できるわけではありません。1年間服用後も飲み続けたほうが進行を緩やかにできるので、副作用がなければ、長期間服用することになります。ただし、すべての人に効果があるわけではなく、3~4割程度の方に有効な薬剤です。
実は、ドネペジルの有効率はもっと高いという報告もあります。
鳥取大学生体制御学・浦上克哉先生の報告では、改善した症状に関して家族から細かく聞き取り調査をして有効率を算出すると、有効率は48%であったそうです(CLINICIAN vol.54 No.563 1122-1129 2007)。
詳しいデータをお知りになりたい方は以下をお読み下さい。
http://www.e-clinician.net/vol54/no563/pdf/sp15_563.pdf
へぇ~! そうなんだ! 検討方法が違うと有効率も違ってくるんだ! 有効率だけ見ていてもダメなんですね?!
そう! だから医療情報を判断することは難しいんだ!
笠間先生の「著効」ってどんな方なんですか?
私は、投薬開始3か月時点で、改訂長谷川式簡易知能評価スケール(HDS-R)が4点以上改善した症例を有効例として、HDS-Rの点数の改善に加えてご家族の印象としても著しく改善した場合を「著効例」としています。
ドネペジルが非常によく効く方というのは、いったいどのような経過を辿るのか、簡単にご紹介します。
81歳の女性は、1995年より認知症の症状が出現しました。1999年には家族の顔さえも分からなくなっていました。物盗られ妄想・徘徊・尿失禁なども出現し、2000年11月1日初めて私の外来を受診されました。初診時の改訂長谷川式簡易知能評価スケール(HDS-R)は30点満点中の10点でした。
ご存じのように、介護保険制度は2000年4月に制度開始になりました。この方は制度が始まってまもなく認定されており、要介護判定は5段階中4番目に重い要介護4でした。
ドネペジル開始後、話が理解できるようになったと家族より喜びの声が聞かれ、また徘徊も消失しました。投薬開始後3か月目のHDS-Rは、15点まで改善していました。しかし、2001年9月に、ご家族の体調不良で通院困難となり、家族の判断でドネペジルを中断したところ、症状はいっきに悪化しHDS-Rは8点まで低下しました。
講演会やメール相談で、時折質問を受けることの一つに、「アリセプトはいつまで続けるのでしょうか?」という質問があります。
この質問に対しては、私は次のように回答しております。
「ドネペジルは、認知機能の低下を3~5年間抑制し続けると考えられています。可能でしたら服薬を継続した方が良いと思います。しかし、継続が困難でしたら一度中断してみて、症状の悪化がないことを確認すれば、中止を検討されても良いと思います。」
えっ?! いったん開始した認知症薬剤が中止できることもあるの?
はい! 手術などで薬が服用できず、中止せざるを得ない場合もありますからね!
でも紹介したケースのように、中止するといっきに症状が悪化するケースもありますから、素人判断で中止することはやめて下さいね。
では、再開するのであればいつまでに再開すれば問題ないのでしょうか。
この点に関して、金沢大学大学院医学系研究科脳老化・神経病態学(神経内科)の山田正仁教授は、「6週以上の休薬では進行抑制効果そのものが消失する可能性がある」と指摘しています(日本医事新報 No.4410 69-73 2008)。最近では、可能であれば休薬期間は3週間以内にとどめるべきという意見もありますので、その辺りを目安に判断して下さいね。
アルツハイマー病は確かに不治の病です。しかし、私自身この3%という数字には支えられています。高齢だからと簡単に諦めずに、治療の道を模索して下さいね。
メモ: 改訂長谷川式認知症スクリーニングテスト(HDS-R)
HDS-Rは、認知症のスクリーニングテストとしてわが国で開発されたもので30点満点です。
通院介助のヘルパー
投稿者:梨木 投稿日時:10/11/26 17:58
著効のあった方がヘルパーと通院・服薬出来ていれば、ご本人様はもとよりご家族の介護負担も軽減されたのでは、と残念に思いました。
その後、介護保険の改定で、医療機関内での付き添いに原則介護ヘルパーは認められなくなりましたが、ヘルパーが一旦帰って又お迎えに行くのも現実的でなく、私の勤務先では、その間自費ヘルパーだけれども割引料金で設定していました。
ただ、利用者様が医師の説明を理解できない強度の難聴・認知症の場合、その理由を主治医様から書面で証明して頂いて、介護保険で対応できた例もありました。自治体で違うでしょうが。
今後介護保険もどんどん制限が増え、創設の理念から離れて行くように見えます。
目の前の支出を少し抑えることで、かえって将来のQOLの低下、介護負担増、医療費増などに結びつくのではと心配しています。
Re:通院介助のヘルパー
投稿者:笠間 睦 投稿日時:10/11/26 22:05
梨木さんへ
この方は、遠方から通院されていた方でした。
通院を中断する前に、私の方に連絡して頂ければ良かったのですが・・。
幸いこの患者さんの場合、その後介護者の方の体調が戻り、比較的早い時期に内服を再開できましたので、服薬中止前の状態に近い状況まで回復することが可能でした。
コメントありがとうございました。
Re:Re:通院介助のヘルパー
投稿者:梨木 投稿日時:10/11/28 10:36
良かったですね。
ご家族様の状況が変わった時、ケアマネジャーや地域包括センターにご相談いただくと、手段があることをお伝えしたく書きました。
AD患者さんにおける感覚器の障害 [アルツハイマー病]
AD患者さんにおける感覚器の障害
周辺視野の問題があって、運転中の事故を起こしやすくなることが指摘されています。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第9回『認知症の中核症状に関する理解を深めましょう─視空間機能障害』(2012年12月20日公開)
3番目は視空間機能障害です。従来の基準で、「失認」・「失行」とされた所見が視空間機能障害としてまとめられました。
地理的障害(地誌的見当識障害)には街並失認(視覚性失認の一型)と道順障害(視空間失認の一型)があります。街並失認とは、街並(建物・風景)の同定障害であり、周囲の風景が道をたどるうえでの目印にならないために道に迷ってしまいます。
自宅付近で道に迷うアルツハイマー病患者の病態としては、少なくとも初期には「道順障害」的な要素が大きいようです(高橋伸佳:街を歩く神経心理学 医学書院, 東京, 2009, pp152-153)。
失認のある患者さんにおいては、お風呂の入り口に床の色と違うバスマットが敷いてあると、バスマットの部分が谷底のように見えてしまい、患者さんは「落ちてしまう」と感じ、渡れない(足が踏み出せない)と訴える現象が出現することもあります。このような症状を呈した場合には、バスマットをどける(谷底をなくす)か、床の色と同じ色のバスマットにするなどの対応が効果的です。
また、視空間機能障害が出現してくると、車庫入れで車を擦ってしまうなどの影響も出てきます。
失行とは、運動障害はなく、手や足が動くのに、まとまった動作や行為ができないことです。挨拶ができないとか、箸などの道具が使えない(箸を渡しても食事を摂取する動作ができない)、使い慣れた電化製品の使用がわからない、図形がうまく書けないなどの不都合が生じます。そのため、日常生活にも差し障りが出てきます。
1995年に46歳で若年性認知症と診断されたクリスティーンさんは、視空間機能障害に絡んで以下のように語っています(一部改変)。
「世界はグラグラした場所に感じられ、その空間の中で自分の体の各部分がどこにあるのかがわかりづらくなる。
液体の入ったコップをこぼさずに持つには大変な努力がいる。コップを見て、自分の体を見て、体がどうなっているか注意しなければならない…。こんな一見単純な作業にも、無数の動作と反応がある。私にとって、飲み物を運ぶのは相当難しい仕事になってしまった。私の体の各部分はどこにあるのか? コップはどこか? どうして注意して見ていないと中の液体がピチャピチャ跳ねるのか? どうしてテーブルの向こうへ運ぶ途中で突然物にぶつかってしまうのか? どうして手を伸ばすと物をひっくり返してシミをつくってしまうのか?
それはちょうど競馬馬の目隠しをつけてトンネルをのぞいているような感じだ。周辺視野は狭くなり、まわりではっきりとした動きがあると、私はすぐにビクッと驚いてしまい、それまでの行動をじゃまされてしまう。まるでウインカーが点滅し続けているみたいだ。鏡の前を通ると、部屋の中に自分と一緒に知らない人がいると思って、跳び上がってしまうこともあるほどだ!
台所や浴室では、よく物をひっくり返す。距離の判断を間違えて、物にぶつかってしまうのだ。模様に惑わされることもある。表面が滑らかでも模様のある床を歩くと、つまづいてしまうことがある。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, pp132-133)
「私たちの不安が増大するひとつの理由は、道がわからない、自分が今いるところがわからないということだ。頭の中の地図をなくしたか、そうでなくとも、地図と自分の周囲の現実とが結びつかなくなってしまったようになる。だから自分の家のまわりの見慣れたところでない限り、誰かに道を案内してもらわなければならない。
2000年5月、私はカウンセリング学位コースの一環として、バサーストの大学の寮にひとりで行った。それはまさに悪夢だった。寮からわずか50メートルほどしか離れていない学生食堂や講義室へ行く道がわからないのだ。とにかく見覚えのある顔(もちろん「名前」ではない─名前なんてまったくわからなかったのだから)の人のあとについて行くしかなかった。ケアパートナーの案内なしに、ひとりで知らないところへ行こうとしたのは、あの時が最後になった。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, p152)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第138回『認知症のケア どうしたらもっとうまく意思疎通できるのか』(2013年5月12日公開)
クリスティーンさんは、ゴールドスミスの本に記載されている記述(Goldsmith M:Hearing the voice of people with dementia, Jessica Kingsley Publishers, London, 1996, pp58-59)を引用し、どうすれば認知症のある人たちともっとうまく意思疎通できるかを紹介しています(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, pp190-191)。以下に列記致します。
・ゆったりした環境をつくる。
・穏やかな、自信に満ちた、気さくな態度をとる。
・その人の視野の内に入り、同じ目の高さで目を合わせたまま、名前を言う。
・その人がいやがらない範囲内で身体にふれる。
・簡単な言葉でゆっくりと、敬意をもって話す。
・理解する時間を与える。
・聞き上手になって、言葉がつかえてもじっと待ち、言葉の裏にある意味を察する。
・あいまいな言い方を避け、短い文章を使う。
・できれば写真などを使って、言っていることを具体的に説明する。
・話について行くように努力し、言い間違いを直したり、不適切な返答を笑ったりしない。
・よくできた時はほめる。
・感情をむきだしにされても、あわてない。
「その人の視野の内に入り、同じ目の高さで目を合わせたまま、名前を言う」という事項に関連して、アルツハイマー病(AD)患者さんにおける視野についての興味深い記述をご紹介しておきましょう。
「ADで、どのような感覚器の障害が起こるかは十分明らかにはなっていませんが、一般的には、視覚、ついで聴覚などの系統発生学的に新しい感覚器の機能から低下すると考えられています。
人間は、外界の情報を得るために80%以上を視覚に頼って生活している生き物だといわれており、認知症が進行すると、視覚の障害に配慮する必要があります。
人間の視野は上下150度、左右200度の範囲に及びますが、私たちは物を注視するとき、網膜の黄斑部のなかにある直径1.85mmの中心窩でほとんどの情報を得ています。この視神経が集中している中心窩を用いて、多くの情報が得られるのは、視野の中心から5度の視野の範囲だといわれています。視野の中心から10度になると情報量は5分の1に、20度に広がると情報量は10分の1にまで低下します。
進行した認知症の方では、なおさら視野の真ん中に必要な情報がないと感知することができません。常にその人の正面に必要な情報が来るように留意します。本人の身体介護の場面でも、真正面から声掛けをしながら近づかなければなりません。」(平原佐斗司編著:認知症ステージアプローチ入門─早期診断、BPSDの対応から緩和ケアまで 中央法規, 東京, 2013, p28)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第231回『注目される自動車運転の問題─視野が次第に狭くなる』(2013年8月18日公開)
『アルツハイマーのための新しいケア─語られなかった言葉を探して』(阿保順子監訳 誠信書房 2007)を読みますと、著者のジョアン・コーニグ・コステさんと夫(40歳代で発症し、1976年死去)の「認知症の世界への旅立ちは、サポートグループもなければマニュアルや指標一つなかった1971年に始まった」(同書p4)と書かれています。全米アルツハイマー病協会が設立(1980年)される約10年も前のことです。
指南書の類が全くなかった時代に、細やかな観察力から「ハビリテーションの五つの鍵」を独自に考案し実践した行動力は本当に驚きです。
「五つの鍵」の4番目である「患者の世界に生きる」とはどういうことでしょうか。「言い返したり叱咤せず、患者の視点で物事をみる。患者の今いる『場所』と『時』を共有し、そのなかでお互いに喜びを見いだす」(同書p9)ことです。多くの介護本が広く出回っている今日でさえ、介護者が「叱らない介護」に到達するまでには長い年月を要する現状を思えば、ジョアンさんの感性の鋭さは容易に窺い知ることができますね。
シリーズ第138回『認知症のケア どうしたらもっとうまく意思疎通できるのか』(http://apital.asahi.com/article/kasama/2013050200010.html)においてご紹介しましたように、人間の視野は上下150度、左右200度の範囲に及びますが、私たちは物を注視するとき、網膜の黄斑部のなかにある直径1.85mmの中心窩でほとんどの情報を得ています。この視神経が集中している中心窩を用いて、多くの情報が得られるのは、視野の中心から5度の視野の範囲だといわれています。視野の中心から10度になると情報量は5分の1に、20度に広がると情報量は10分の1にまで低下します。進行した認知症の方では、なおさら視野の真ん中に必要な情報がないと感知することができない(平原佐斗司編著:認知症ステージアプローチ入門─早期診断、BPSDの対応から緩和ケアまで 中央法規, 東京, 2013, p28)のでしたね。
運転能力に特に大きく関与するのが「有効視野」とされています。「自動車運転の場合に限らず、視覚認知は周辺視によって次の注視すべき対象を検出した後、それを中心視で詳しく確認し、また次の対象物を検出するという作業の繰り返しである。この周辺視のうち、認知に寄与する部分が有効視野に該当する。有効視野という概念はMackworthにより、『ある視覚課題の遂行中に、注視点の周りで情報が瞬間的に蓄えられ、読み出される部分』と定義されている。視力、視野、コントラスト感度、有効視野、認知機能などと事故との関連を検討した結果、交通事故を予測する上で最も予測力が高いものは有効視野であった。」(一部改変)と報告されています(藤田佳男:有効視野を用いた運転能力評価法について教えてください. Geriatric Medicine Vol.50 179-181 2012)。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第232回『注目される自動車運転の問題─競馬馬の目隠しをつけてトンネルをのぞく感じ』(2013年8月19日公開)
「有効視野」と聞きますと、私は、眼球運動異常とアルツハイマー病との関係を研究した報告(http://lib.nagaokaut.ac.jp/kiyou/data/study/k24/K24_8.pdf)を思い出します。
特定のターゲットの探索に関与しているのは、前頭眼野という部位です(ダーリア・W・ザイデル:芸術的才能と脳の不思議─神経心理学からの考察 河内十郎監訳,河内薫訳 医学書院, 2010, p189)。
若年性認知症を患ったクリスティーンさんは、視野の制限について以下のように語っています。
「競馬馬の目隠しをつけてトンネルをのぞいているような感じだ。周辺視野は狭くなり、まわりではっきりとした動きがあると、私はすぐにビクッと驚いてしまい、それまでの行動をじゃまされてしまう。まるでウインカーが点滅し続けているみたいだ。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, p132)
また、クリスティーンさんは、車を運転することの難しさについても言及しております(一部改変)。
「あなたに認知症があって、まだ車の運転をしているならば、いつまでそんなふうに人に頼らずにやっていけるのかと考えるだろう。ちょっと車が接触しただけでも、みんなから認知症のせいにされないだろうかと心配になる。車の運転をあきらめることは、認知症の人とその家族にとって、深い心の傷になる。現在、私は緊急時だけ運転することにしているが、我が家のある静かな田舎でも、家から二つ三つ通りを行くだけで私はとても不安になる。不測の事態に対して絶対に素早く反応できないと思うし、目先の道路に焦点を定めて集中するのはとても難しい。さらには、すべてのペダル、レバー、文字盤、ライトを覚えて、それらがどう動くのか、何のためのものか、そして自分が次にすべきことは何なのか、覚えておかなくてはならないのは大変なことなのだ。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, pp133-134)
では、有効視野が低下してくるとどのような交通事故を起こしやすくなってくるのでしょうか。
「通常、我々は運転中、視線を向けて網膜の中心で事物を捉える中心視とその周辺の情報にも注意を配る周辺視との両者を同時並行している。有効視野(Useful Field of View;UFOV)検査では、中心視と同時に意識でき、すばやい課題反応に活かされる周辺視野の範囲(有効視野)を評価する。Clayらによるメタ分析では、UFOV検査と否定的な運転行動の生起との関連が十分な効果量をもって(Cohen's d=0.95)示されている。高齢者では若齢者に比べて、放射方向へ周辺距離が増すにつれてUFOV課題の成績が低下する有効視野の狭隘が生じる。こうした有効視野の狭隘を本質とした視空的注意の障害は、交差点で出会い頭に衝突する事故が多いとされる高齢運転者一般の危険運転をよく説明するものであり、エビデンスも蓄積されている。」(河野直子:認知機能低下と運転適性:一般及び軽度認知障害の高齢運転者を対象とした研究動向. Dementia Japan Vol.27 191-198 2013)
メモ:Cohen's d
2グループの平均値の差を比較するt検定という手法があります。この手法では、効果量(Effect Size)として、dという指標を使います。dが0.2より大きいとき効果量は小さい(small)と言い、dが0.5より大きいとき効果量は中くらい(medium)と言い、dが0.8より大きいとき効果量は大きい(large)と言います(http://www.mizumot.com/method/mizumoto-takeuchi.pdf)。
周辺視野の問題があって、運転中の事故を起こしやすくなることが指摘されています。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第9回『認知症の中核症状に関する理解を深めましょう─視空間機能障害』(2012年12月20日公開)
3番目は視空間機能障害です。従来の基準で、「失認」・「失行」とされた所見が視空間機能障害としてまとめられました。
地理的障害(地誌的見当識障害)には街並失認(視覚性失認の一型)と道順障害(視空間失認の一型)があります。街並失認とは、街並(建物・風景)の同定障害であり、周囲の風景が道をたどるうえでの目印にならないために道に迷ってしまいます。
自宅付近で道に迷うアルツハイマー病患者の病態としては、少なくとも初期には「道順障害」的な要素が大きいようです(高橋伸佳:街を歩く神経心理学 医学書院, 東京, 2009, pp152-153)。
失認のある患者さんにおいては、お風呂の入り口に床の色と違うバスマットが敷いてあると、バスマットの部分が谷底のように見えてしまい、患者さんは「落ちてしまう」と感じ、渡れない(足が踏み出せない)と訴える現象が出現することもあります。このような症状を呈した場合には、バスマットをどける(谷底をなくす)か、床の色と同じ色のバスマットにするなどの対応が効果的です。
また、視空間機能障害が出現してくると、車庫入れで車を擦ってしまうなどの影響も出てきます。
失行とは、運動障害はなく、手や足が動くのに、まとまった動作や行為ができないことです。挨拶ができないとか、箸などの道具が使えない(箸を渡しても食事を摂取する動作ができない)、使い慣れた電化製品の使用がわからない、図形がうまく書けないなどの不都合が生じます。そのため、日常生活にも差し障りが出てきます。
1995年に46歳で若年性認知症と診断されたクリスティーンさんは、視空間機能障害に絡んで以下のように語っています(一部改変)。
「世界はグラグラした場所に感じられ、その空間の中で自分の体の各部分がどこにあるのかがわかりづらくなる。
液体の入ったコップをこぼさずに持つには大変な努力がいる。コップを見て、自分の体を見て、体がどうなっているか注意しなければならない…。こんな一見単純な作業にも、無数の動作と反応がある。私にとって、飲み物を運ぶのは相当難しい仕事になってしまった。私の体の各部分はどこにあるのか? コップはどこか? どうして注意して見ていないと中の液体がピチャピチャ跳ねるのか? どうしてテーブルの向こうへ運ぶ途中で突然物にぶつかってしまうのか? どうして手を伸ばすと物をひっくり返してシミをつくってしまうのか?
それはちょうど競馬馬の目隠しをつけてトンネルをのぞいているような感じだ。周辺視野は狭くなり、まわりではっきりとした動きがあると、私はすぐにビクッと驚いてしまい、それまでの行動をじゃまされてしまう。まるでウインカーが点滅し続けているみたいだ。鏡の前を通ると、部屋の中に自分と一緒に知らない人がいると思って、跳び上がってしまうこともあるほどだ!
台所や浴室では、よく物をひっくり返す。距離の判断を間違えて、物にぶつかってしまうのだ。模様に惑わされることもある。表面が滑らかでも模様のある床を歩くと、つまづいてしまうことがある。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, pp132-133)
「私たちの不安が増大するひとつの理由は、道がわからない、自分が今いるところがわからないということだ。頭の中の地図をなくしたか、そうでなくとも、地図と自分の周囲の現実とが結びつかなくなってしまったようになる。だから自分の家のまわりの見慣れたところでない限り、誰かに道を案内してもらわなければならない。
2000年5月、私はカウンセリング学位コースの一環として、バサーストの大学の寮にひとりで行った。それはまさに悪夢だった。寮からわずか50メートルほどしか離れていない学生食堂や講義室へ行く道がわからないのだ。とにかく見覚えのある顔(もちろん「名前」ではない─名前なんてまったくわからなかったのだから)の人のあとについて行くしかなかった。ケアパートナーの案内なしに、ひとりで知らないところへ行こうとしたのは、あの時が最後になった。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, p152)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第138回『認知症のケア どうしたらもっとうまく意思疎通できるのか』(2013年5月12日公開)
クリスティーンさんは、ゴールドスミスの本に記載されている記述(Goldsmith M:Hearing the voice of people with dementia, Jessica Kingsley Publishers, London, 1996, pp58-59)を引用し、どうすれば認知症のある人たちともっとうまく意思疎通できるかを紹介しています(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, pp190-191)。以下に列記致します。
・ゆったりした環境をつくる。
・穏やかな、自信に満ちた、気さくな態度をとる。
・その人の視野の内に入り、同じ目の高さで目を合わせたまま、名前を言う。
・その人がいやがらない範囲内で身体にふれる。
・簡単な言葉でゆっくりと、敬意をもって話す。
・理解する時間を与える。
・聞き上手になって、言葉がつかえてもじっと待ち、言葉の裏にある意味を察する。
・あいまいな言い方を避け、短い文章を使う。
・できれば写真などを使って、言っていることを具体的に説明する。
・話について行くように努力し、言い間違いを直したり、不適切な返答を笑ったりしない。
・よくできた時はほめる。
・感情をむきだしにされても、あわてない。
「その人の視野の内に入り、同じ目の高さで目を合わせたまま、名前を言う」という事項に関連して、アルツハイマー病(AD)患者さんにおける視野についての興味深い記述をご紹介しておきましょう。
「ADで、どのような感覚器の障害が起こるかは十分明らかにはなっていませんが、一般的には、視覚、ついで聴覚などの系統発生学的に新しい感覚器の機能から低下すると考えられています。
人間は、外界の情報を得るために80%以上を視覚に頼って生活している生き物だといわれており、認知症が進行すると、視覚の障害に配慮する必要があります。
人間の視野は上下150度、左右200度の範囲に及びますが、私たちは物を注視するとき、網膜の黄斑部のなかにある直径1.85mmの中心窩でほとんどの情報を得ています。この視神経が集中している中心窩を用いて、多くの情報が得られるのは、視野の中心から5度の視野の範囲だといわれています。視野の中心から10度になると情報量は5分の1に、20度に広がると情報量は10分の1にまで低下します。
進行した認知症の方では、なおさら視野の真ん中に必要な情報がないと感知することができません。常にその人の正面に必要な情報が来るように留意します。本人の身体介護の場面でも、真正面から声掛けをしながら近づかなければなりません。」(平原佐斗司編著:認知症ステージアプローチ入門─早期診断、BPSDの対応から緩和ケアまで 中央法規, 東京, 2013, p28)
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第231回『注目される自動車運転の問題─視野が次第に狭くなる』(2013年8月18日公開)
『アルツハイマーのための新しいケア─語られなかった言葉を探して』(阿保順子監訳 誠信書房 2007)を読みますと、著者のジョアン・コーニグ・コステさんと夫(40歳代で発症し、1976年死去)の「認知症の世界への旅立ちは、サポートグループもなければマニュアルや指標一つなかった1971年に始まった」(同書p4)と書かれています。全米アルツハイマー病協会が設立(1980年)される約10年も前のことです。
指南書の類が全くなかった時代に、細やかな観察力から「ハビリテーションの五つの鍵」を独自に考案し実践した行動力は本当に驚きです。
「五つの鍵」の4番目である「患者の世界に生きる」とはどういうことでしょうか。「言い返したり叱咤せず、患者の視点で物事をみる。患者の今いる『場所』と『時』を共有し、そのなかでお互いに喜びを見いだす」(同書p9)ことです。多くの介護本が広く出回っている今日でさえ、介護者が「叱らない介護」に到達するまでには長い年月を要する現状を思えば、ジョアンさんの感性の鋭さは容易に窺い知ることができますね。
シリーズ第138回『認知症のケア どうしたらもっとうまく意思疎通できるのか』(http://apital.asahi.com/article/kasama/2013050200010.html)においてご紹介しましたように、人間の視野は上下150度、左右200度の範囲に及びますが、私たちは物を注視するとき、網膜の黄斑部のなかにある直径1.85mmの中心窩でほとんどの情報を得ています。この視神経が集中している中心窩を用いて、多くの情報が得られるのは、視野の中心から5度の視野の範囲だといわれています。視野の中心から10度になると情報量は5分の1に、20度に広がると情報量は10分の1にまで低下します。進行した認知症の方では、なおさら視野の真ん中に必要な情報がないと感知することができない(平原佐斗司編著:認知症ステージアプローチ入門─早期診断、BPSDの対応から緩和ケアまで 中央法規, 東京, 2013, p28)のでしたね。
運転能力に特に大きく関与するのが「有効視野」とされています。「自動車運転の場合に限らず、視覚認知は周辺視によって次の注視すべき対象を検出した後、それを中心視で詳しく確認し、また次の対象物を検出するという作業の繰り返しである。この周辺視のうち、認知に寄与する部分が有効視野に該当する。有効視野という概念はMackworthにより、『ある視覚課題の遂行中に、注視点の周りで情報が瞬間的に蓄えられ、読み出される部分』と定義されている。視力、視野、コントラスト感度、有効視野、認知機能などと事故との関連を検討した結果、交通事故を予測する上で最も予測力が高いものは有効視野であった。」(一部改変)と報告されています(藤田佳男:有効視野を用いた運転能力評価法について教えてください. Geriatric Medicine Vol.50 179-181 2012)。
朝日新聞アピタル「ひょっとして認知症-PartⅡ」第232回『注目される自動車運転の問題─競馬馬の目隠しをつけてトンネルをのぞく感じ』(2013年8月19日公開)
「有効視野」と聞きますと、私は、眼球運動異常とアルツハイマー病との関係を研究した報告(http://lib.nagaokaut.ac.jp/kiyou/data/study/k24/K24_8.pdf)を思い出します。
特定のターゲットの探索に関与しているのは、前頭眼野という部位です(ダーリア・W・ザイデル:芸術的才能と脳の不思議─神経心理学からの考察 河内十郎監訳,河内薫訳 医学書院, 2010, p189)。
若年性認知症を患ったクリスティーンさんは、視野の制限について以下のように語っています。
「競馬馬の目隠しをつけてトンネルをのぞいているような感じだ。周辺視野は狭くなり、まわりではっきりとした動きがあると、私はすぐにビクッと驚いてしまい、それまでの行動をじゃまされてしまう。まるでウインカーが点滅し続けているみたいだ。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, p132)
また、クリスティーンさんは、車を運転することの難しさについても言及しております(一部改変)。
「あなたに認知症があって、まだ車の運転をしているならば、いつまでそんなふうに人に頼らずにやっていけるのかと考えるだろう。ちょっと車が接触しただけでも、みんなから認知症のせいにされないだろうかと心配になる。車の運転をあきらめることは、認知症の人とその家族にとって、深い心の傷になる。現在、私は緊急時だけ運転することにしているが、我が家のある静かな田舎でも、家から二つ三つ通りを行くだけで私はとても不安になる。不測の事態に対して絶対に素早く反応できないと思うし、目先の道路に焦点を定めて集中するのはとても難しい。さらには、すべてのペダル、レバー、文字盤、ライトを覚えて、それらがどう動くのか、何のためのものか、そして自分が次にすべきことは何なのか、覚えておかなくてはならないのは大変なことなのだ。」(クリスティーン・ブライデン:私は私になっていく─痴呆とダンスを 馬籠久美子・桧垣陽子訳, クリエイツかもがわ, 2004, pp133-134)
では、有効視野が低下してくるとどのような交通事故を起こしやすくなってくるのでしょうか。
「通常、我々は運転中、視線を向けて網膜の中心で事物を捉える中心視とその周辺の情報にも注意を配る周辺視との両者を同時並行している。有効視野(Useful Field of View;UFOV)検査では、中心視と同時に意識でき、すばやい課題反応に活かされる周辺視野の範囲(有効視野)を評価する。Clayらによるメタ分析では、UFOV検査と否定的な運転行動の生起との関連が十分な効果量をもって(Cohen's d=0.95)示されている。高齢者では若齢者に比べて、放射方向へ周辺距離が増すにつれてUFOV課題の成績が低下する有効視野の狭隘が生じる。こうした有効視野の狭隘を本質とした視空的注意の障害は、交差点で出会い頭に衝突する事故が多いとされる高齢運転者一般の危険運転をよく説明するものであり、エビデンスも蓄積されている。」(河野直子:認知機能低下と運転適性:一般及び軽度認知障害の高齢運転者を対象とした研究動向. Dementia Japan Vol.27 191-198 2013)
メモ:Cohen's d
2グループの平均値の差を比較するt検定という手法があります。この手法では、効果量(Effect Size)として、dという指標を使います。dが0.2より大きいとき効果量は小さい(small)と言い、dが0.5より大きいとき効果量は中くらい(medium)と言い、dが0.8より大きいとき効果量は大きい(large)と言います(http://www.mizumot.com/method/mizumoto-takeuchi.pdf)。
笠間 睦:メマンチンによるアルツハイマー病の中核症状に対する効果判定の試み─MoCA-Jを用いて─. Geriatric Medicine Vol.51 723-727 2013 [アルツハイマー病]

語り 040
─最初に「どうも自分は人の名前を忘れたりして変だな」って思ってから、今日まで、忘れやすさに何か変化はありますか?
「だんだん忘れるようになったな」とは思うてたんですけども、メマリーっちゅう薬を飲まんようになったら、急に、忘れることが多くなった。検査の
結果、やめたほうがいいんじゃないかっちゅうことで、もうお薬を出してもらえやんようになったんです。
─お薬を出してもらえなくなったことについて、どう思いましたか?
そのときはそんなにもの忘れがひどくなるとは思いませんだもんで、あれですけど……。考えてみたら、あのお薬が今まで効いとったんかなと思う。
─そのお薬をやめて、「もの忘れが前よりもひどくなったな」って思うのは、お薬を飲んでいるときは「調子がよくなったな。前よりも忘れなくなったな」っていう感覚はあったんですね。
薬を飲んどると、それ〔もの忘れの進み方〕が遅なるちゅうか……。よくなったとは感じません。治る薬じゃないもんで。そでけんども、薬がなくなってから気がつきました、今まではあの薬のおかげやったなって。それ飲んでなかったら、もっとずっとその先がひどくなってたかもわかりませんわね。
本人12(プロフィール:p.613)
【認知症の語り─本人と家族による200のエピソード. 健康と病いの語りディペックス・ジャパン, 東京, 2016, pp111-112】
私の感想:
メマンチン(メマリー
メマンチンの中核症状に対する効果をsevere impairment battery(SIB)で評価(国内第Ⅲ相試験-IE3501)したところ、4つの領域(言語,注意,実行,視空間能力)で有意な改善を認めております。
要するに、注意機能が向上し記憶が良くなったように感じるのです。
詳細は、私の論文(『老年医学』2013)に記載されておりますのでご参照下さい。
笠間 睦:メマンチンによるアルツハイマー病の中核症状に対する効果判定の試み─MoCA-Jを用いて─. Geriatric Medicine Vol.51 723-727 2013
はじめに
認知症における最大のリスクは「加齢」とされており,超高齢社会の到来とともに,認知症,特にアルツハイマー病は「ありふれた疾患」の1つになってきている.このような時代を背景として,対症治療ではあるが4種類のアルツハイマー型認知症治療薬が汎用されるようになった.そのため,認知症専門医だけでなくかかりつけ医が認知症診療に積極的に関わっていくことが求められている.
しかしながら,奈良市においてかかりつけ医300人を対象として実施されたアンケート調査で,認知症治療の問題点として,実にかかりつけ医の52.8%が「薬の効果がはっきりしない」と回答している1).その理由は明らかでないが,プラセボ効果2)・ノセボ効果3)の影響,効果判定方法の相違なども一因と考えられる.実際に,個々の症例で認知症の程度や内容,進行速度は異なっており,治療開始前からの効果判定ポイントが明確でなかったりすることも一因となろう.
そこで筆者は,かかりつけ医がその効果を実感できるような指標の導入が必要と考え,日常臨床の現場でも実施可能な評価方法として,改訂長谷川式認知症スクリーニングテスト(HDS-R)とともに日本語版モントリオール認知評価検査(Montreal Cognitive Assessment:MoCA-J)を用いてアルツハイマー病患者における中核症状の評価を試みた.MoCA-Jは,多領域の認知機能(注意機能,集中力,実行機能,記憶,言語,視空間認知,概念的思考,計算,見当識)について,約10分という短い時間で評価することが可能である4).
なお,今回用いた治療薬はメマンチンであり,その中核症状に対する効果としては,severe impairment battery(SIB)で領域別認知機能を評価(国内第Ⅲ相試験-IE3501)したところ,4つの領域(言語,注意,実行,視空間能力)で有意な改善が認められている5).しかし,SIBによる評価を多忙な日常診療の現場で定期的に実施することは困難であり,メマンチンによる中核症状の改善を客観的に捉えにくい要因の1つとなっている.
以上の理由から,MoCA-Jを用いてアルツハイマー病の中核症状に対するメマンチンの効果判定を試みた.
対象と方法
対象は2013年1~2月に榊原白鳳病院物忘れ外来を受診してアルツハイマー病と診断され,メマンチン投与を開始した連続5症例(年齢:50歳代1例,70歳代4例,性別:男1例,女4例)である.なお,アルツハイマー病の診断はDSM-Ⅳに基づいて行った.これらの臨床像(教育歴,既往歴,治療歴,合併症,併用薬,現病歴,生活歴,ADL,認知症の行動・心理症状[behavioral and psychological symptoms of dementia:BPSD]の有無・程度など)を医療面接で聴取後,本研究について説明し,同意を得て,メマンチンを所定の用量,用法で投与した.メマンチン投与前および投与後4週目(ChEIとの併用例においては8週目)に日本語版MoCA-Jを実施し,中核症状に対するメマンチンの効果を評価した.なお,メマンチンの維持量に関しては,副作用がみられない限り20mgまで増量した.
結果
1.対象の臨床像
今回の5例は,全例ともにChEI(ドネペジル,ガランタミン,リバスチグミン)による治療を受けていた.しかし,その治療効果を実感できず筆者の物忘れ外来を受診した経緯である.
ChEIによる治療期間は,8~31カ月(平均20カ月)であった.
5例全例において,記銘記憶障害が認められている.
なお,5例のクレアチニンクリアランス推定値(Cockcroft-Gault計算式による)は,42mL/min,74mL/min,71mL/min,91mL/min,59mL/minであり,30mL/min以下の症例はなく腎機能は全例において正常である.
事例1から5のプロフィールを以下に簡単に紹介する.
【事例1 79歳女性 教育歴:9年】
夫と2人暮らし.娘2人が近隣に住んでおり,通院の際には付き添いとして来院している.
70歳まで経理の仕事に従事(最後の15年間は取締役を務めた).
X-3年,道順障害が出現してきた.X-2年になると手の込んだ料理が困難となってきた.
X年,もの忘れが目立つようになり,易刺激性および夫に対する暴言も出現してきたため当院を初診.道順障害のため,1人で外出すると目的地にたどり着けないことが目立つ状況である.また,居住区内にある公共のコピー機の使い方が分からず,カッとなって叩いて壊してしまい,居住区で問題となったことがある.夫が運転する車に同乗して買い物に行き,料理は本人が作ってはいるものの,連日のように煮物料理ばかりが続く状況である.
ガランタミンにて8カ月治療したものの期待した効果が認められず,メマンチンを併用開始とした.
【事例2 59歳女性 教育歴:12年】
若年発症のアルツハイマー型認知症である.夫と2人暮らし.子供2人は社会人となって家を出ている.同一敷地内に義父母が住んでいる.
X-3年,仕事の間違いが多くなり退職勧奨され郵便局を辞めている.X-2年になると料理をほとんどしなくなり,同一敷地内に住む義母が煮物などを作り持参する状況となった.精査目的にて神経内科を受診したところ,初診日に意に反して病名告知を受け,医師との相性が合わなかったことから,それ以降は近くのかかりつけ医にてドネペジル5mg(ジェネリック)を処方されてきた.
知人の勧めにより,X年に当院を初診.夫から聴取した話によると,最近は火の消し忘れが多くなり,不慣れな場所に出掛けると家に帰れない状況である.また,視空間機能障害のためか車庫入れの際にしばしばガレージに接触するようになり,車の運転は控えるようになっている.
目立ったBPSDは認められておらず,現状においては介護保険は申請していない.
【事例3 76歳女性 教育歴:12年】
夫と2人暮らし.X-1年11月,孫を連れて息子夫婦と家族旅行をした際に,前日にした話と全く同じ話をまるで初めてのように話していることに息子が気づいた.X-1年12月,親戚から預かった孫へのプレゼントを持参する約束を忘れていたため本人に確認すると,プレゼントは預かっていないと言い張ることがあった.また前日と同じメニューの料理が出てくるようにもなり,息子がメール医療相談を通して筆者に相談を寄せて,X年1月に当院を初診.ドネペジル5mgにて1年間治療を続けたものの期待した効果が認められず,易刺激性も認められるためメマンチンの併用を開始した.
【事例4 75歳男性 教育歴:12年】
妻と2人暮らし.
高校卒業後,航空自衛隊に入隊した.自衛隊においては教官も務め,55歳にて定年退職.その後,民間の会社に5年間勤め,60歳にて退職している.
X-2年に,かかりつけ医にてアルツハイマー型認知症と診断を受け,ドネペジル5mg(ジェネリック)を処方されている.
記銘記憶障害が徐々に進行しており,精査目的にてX年10月に当院を初診.前医の診断は正しいことを告げ,アルツハイマー型認知症の自然経過について説明し,ドネペジル5mgの服薬を続けて経過をみるように勧めた.
X+1年1月になると,入浴したことを忘れて風呂に入っていないと言ったり,食事をしたことを忘れて食べていないと言うことがしばしば出現してきた.また,毎日訪問していた息子や娘の家がどこか分からないといった状況も出現し,アパシーも目立つため再診となった.HDS-Rが初診時よりも4点悪化しており,易刺激性も認められるためメマンチンを併用開始するとともに,介護保険の申請も勧めた(要介護1と認定された).
【事例5 79歳女性 教育歴:12年】
夫が亡くなってから独居生活であり子供はいない.70歳まで種々のパート勤務をこなしていた.近くに住む妹が車を運転し買い物に連れ出してくれており,また,1日置きに宅配の弁当を頼んで何とか1人暮らしを続けている.
X-1年頃より,物忘れと喚語困難(語想起障害)が目立つようになってきた.X年に,精査目的にて当院を初診.アルツハイマー型認知症と診断し,ドネペジル5mgによる治療を開始した.
X+3年,リバーミード行動記憶検査(RBMT)の標準プロフィール点(24点満点)・スクリーニング点(12点満点)が両者ともに0点になり,作業療法士からはドネペジルの服薬忘れが目立っているとの情報が入り,メマンチンの併用を開始した.
本例においては,BPSDは目立たないものの,数分おきに同じ質問を繰り返すため,近所に住む兄弟にとっては介護負担を感じる大きな要因となっている.介護保険も申請しており,要支援1と認定されている.
2.メマンチン投与後の経過
メマンチンの維持量に関しては,副作用がない限り20mgまで増量することを基本としているが,事例1においては15mgの段階にてめまい感を訴えたため,維持量を10mgとして検討した.5例中3例(事例1,3,4)では,BPSD(易刺激性・情緒不安定)のために家族が介護面で苦慮していたが,メマンチン投与により2例(事例1,3)においてBPSDの軽減・消失を認めた.
今回の5例においては,メマンチン投与により臨床症状として言語障害,視空間機能障害,実行機能障害などの中核症状が改善したケースはなかった.
3.メマンチン投与前後のMoCA-Jの推移
メマンチン投与前後のMoCA-Jの推移を表1に示す.下位項目の点数変化に着目してみると,事例1・3・4においては視空間機能の改善が認められた.事例2・3においては言語機能の改善が認められており,事例3ではMoCA-Jが4点改善していた.また,事例4においては,注意機能の改善が認められている.
言語機能の語想起課題(11個以上で得点)の素点の変化に注目すると,事例1(11点→13点),事例2(6点→11点),事例3(8点→15点),事例4(14点→16点),事例5(4点→6点)といずれも点数は向上しており,臨床的な症状の改善としては捉えられないものの機能的には向上していることが示唆された.
一方で,視空間機能の点数が低下しているケース(事例5)も1例認められた.
考察
対象症例が極めて少ないがMoCA-Jを用いてアルツハイマー病の中核症状に対するメマンチンの効果判定を試みたところ,HDS-Rでは明らかでなかった効果がMoCA-Jで明らかにされた.その理由は効果判定基準による可能性もある.すなわち,長谷川によれば,HDS-R1~2点の小変化は施行時の状況差によっても発生するという.しかし,4~5点の差があれば,まず臨床的にも明らかな改善ないし悪化の所見に関連すると考えられることが報告されており6),本研究でもHDS-R4点以上を「改善」と判定しているからである.
ちなみに,筆者による2011年6月~2012年4月までにメマンチンを投与した連続23例の検討では,HDS-Rが4点以上改善したケースは4例(4/23:17.4%)あった.臨床症状として中核症状の改善が認められた4例のうち,HDS-Rが4点以上改善していたケースは1例のみであり,HDS-Rの改善と中核症状の改善との間には乖離が認められた7).記憶や見当識の評価項目が重視されているHDS-R,mini-mental state examination(MMSE)などの簡易認知機能検査では,メマンチンによる中核症状の改善を的確にとらえることは困難であるのかもしれない.
なお前述の23例の検討において,HDS-Rが4点以上改善した4例,臨床症状として中核症状の改善が認められた4例はいずれも,メマンチンの維持量が20mg/日であった.23例の中には,BPSDが改善した時点でメマンチンの漸増を中止した事例が6例,有害事象(傾眠および便秘)出現のため15mgから10mgに減量して維持した事例が1例,症状不変により家族の希望で中止した事例が1例含まれており,20mgまで増量した15例を対象として評価すると,中核症状の改善率(HDS-R≧4の改善)は26.7%(4/15)であった.なお,今回の5例の検討においては,HDS-Rが4点以上改善した事例はなかった.
一方,本研究のMoCA-Jによる評価では,視空間機能および言語機能がともに2点改善したことにより,点数が20点から24点へと4点改善した事例もあった.MoCAは,軽度アルツハイマー型認知症のスクリーニング検査として感度が高く,MoCA25点をカットオフ値とした場合の感度は100%と報告されている8).今回対象となった5症例においては,メマンチン投与前のMoCA-Jは全例20点以下であり,カットオフ値を5点以上下回る例が対象となっている.
以上より,MoCA-Jはかかりつけ医がアルツハイマー病の中核症状(特に言語,注意,実行,視空間能力)を評価し,メマンチンの投与前後で比較すれば,その効果を実感できる可能性があることが示唆された.
一般に,メマンチンの作用機序は,N-methyl-D-aspartate(NMDA)受容体拮抗作用により,神経細胞内への過剰なCaイオンの流入抑制による神経細胞保護効果と,シナプティックノイズの抑制による記憶・学習機能障害抑制作用である.国内第Ⅲ相試験(IE3501)におけるSIBのスコア変化量でも,投与4週後以降,メマンチンはプラセボ群に対して有意に進行を抑制していた5).また,メマンチンとドネペジルとを併用した場合には,投与4~8週後に効果が発現するとも報告されている9).
メマンチンはまた,NMDA受容体に対する非競合的拮抗作用によって,認知機能を損なうことなくBPSDに効果を示す10).特に,興奮・攻撃性,妄想,易刺激性・情緒不安定において有効性が高く,また,試験開始時には上記の症状を認めなかった患者群においても,メマンチン投与により後の症状発現率が有意に低下したことが報告されている11).
当院物忘れ外来においては,介護者ケアといった視点を重視して種々の取り組みを実施してきた12).介護者の話をじっくり傾聴していると,介護負担における最大の要因は,中核症状のもの忘れではなくBPSDであることを痛感する.認知症患者の介護者においては28~55%が抑うつ状態にあるとされ,その負担度を死亡リスクでみると,がん患者の介護者と比べてもなお高いことが報告されている13).
今後爆発的な増加が予想される認知症患者をできるかぎり地域でみていくためには,BPSDに対する対応強化が喫緊の課題である.この点で非定型抗精神病薬が認知症診療の現場において従来よく用いられてきた.しかしながら,非定型抗精神病薬の使用により死亡率が1.6~1.7倍高くなるとして,2005年にFDAが警告を発している.FDAは2008年には,認知症関連の高齢患者に対する定型・非定型抗精神病薬の使用は,ともに死亡リスク上昇と関連することを通知しており,米国においてはアルツハイマー病に対して禁忌となっている14).このような背景もあって,メマンチンによるBPSD改善への期待は高くなっているのが現状である.
結論
メマンチンによるBPSDの改善効果は肌で感じているものの,中核症状に対する効果を実感している臨床医はまだまだ少ないのが現状である.
MoCA-Jを日常診療において活用することにより,中核症状に対するメマンチンの効果をかかりつけ医が実感できる可能性が示唆された.今後さらに症例数を増やし,より詳細な検討を行いたいと考えている.
参考文献
1)本間 昭:認知症の人のために専門医ができること. 老年精医誌 2013;24(Suppl 1):133-138.
2)本間 昭:認知症患者にプラセボ効果が認められる理由. 日本医事新報 2011;No4573:56-57.
3)笠間 睦:臨床医からみたジェネリック医薬品─認知症治療. Prog Med 2013;33:1089-1092.
4)鈴木宏幸, 藤原佳典:Montreal Cognitive Assessment(MoCA)の日本語版作成とその有効性について. 老年精医誌 2010;21:198-202.
5)第一三共株式会社:医薬品インタビューフォーム メマリー錠
6)長谷川和夫:痴呆の重症度と長谷川式スケール得点. 日本医事新報 1997;No3817:114.
7)笠間 睦:認知症診療におけるメマンチンの位置づけ─自験23例の検討結果─. Prog Med 2013;33:311-315.
8)Nasreddine ZS et al:The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J Am Geriatr Soc 2005;53:695-699.
9)Tariot PN et al:Memantine treatment in patients with moderate to severe Alzheimer disease already receiving donepezil: a randomized controlled trial. JAMA 2004;291:317-324.
10)藤本健一:メマンチン. 日本臨牀 2011;69(Suppl 10):41-46.
11)Gauthier S et al:Effects of memantine on behavioural symptoms in Alzheimer's disease patients: an analysis of the Neuropsychiatric Inventory (NPI) data of two randomised, controlled studies. Int J Geriatr Psychiatry 2005;20:459-464.
12)笠間 睦:認知症介護者に対する終末期の意向調査. 日本医事新報 2011;No4566:26-29.
13)Christakis NA, Allison PD:Mortality after the hospitalization of a spouse. N Engl J Med 2006;354:719-730.
14)遠藤英俊:認知症の薬物療法の実際とその効果. 日医雑誌 2012;141:555-559.



